Продукція
Препарати зареєстровані в Україні
ДИФЕРЕНЦІЙОВАНИЙ ПІДХІД ДО ЛІКУВАННЯ ОСТЕОАРТРОЗУ З КОМОРБІДНОЮ ПАТОЛОГІЄЮ
Шуба Н.М., Воронова Т.Д., Крилова А.С., Хамбір Т.С., Пилипенко А.В.
Резюме. У статті наведена характеристика найбільш поширених лікарських засобів при лікуванні пацієнтів із остеоартрозом — нестероїдних протизапальних препаратів і симптоматичних протизапальних препаратів, зокрема німесуліду, мелоксикаму, діацереїну, хондроїтин сульфату, глюкозаміну сульфату, екстракту кореня імбиру. Описана їх ефективність за показниками суглобового синдрому, а саме ВАШ, індексів Лекена, WOMAC. Досліджено вплив на рівень цитокінів (IL-1β, TNF-α, IGF-1, TGF-β), вільних радикалів (NO), а також вивчено можливість застосування при коморбідній патології та вплив на показники пуринового, вуглеводного та ліпідного обмінів.
ВСТУП
Остеоартроз (ОА) — найбільш поширене та інвалідизуюче захворювання суглобів у світі. За даними National Health and Nutrition Examination Survey (NHANE), суглобова патологія займає третє місце за поширеністю серед хронічних станів у осіб віком старше 65 років (50% випадків) (CDC, 2001). При цьому в структурі інвалідності артриту і болю в нижній ділянці спині належать перша і друга позиція — 17,9 і 16,9% відповідно. Поширеність ОА підвищується з кожним роком, за результатами епідеміологічних досліджень у США протягом останнього десятиліття зросла з 21 до 27 млн осіб серед дорослого населення (Plotnikoff R., 2015).
Поширеність ОА значно вища у людей похилого віку, з коморбідними метаболічними порушеннями, у тому числі ожирінням, гіперурикемією, цукровим діабетом. За останні роки встановлено, що коморбідна патологія істотно погіршує порушення фізичної функції та спричиняє вищу смертність у хворих на ОА (Nü esch E. et al., 2011).
ОА вдвічі частіше розвивається при надмірній масі тіла, індекс маси тіла (ІМТ) >27 кг/м² підвищує ризик ОА на 15% (Шуба Н.М. та співавт., 2012). Збільшення маси жирової тканини призводить до акумуляції клітин запалення та, особливо, макрофагів, які секретують прозапальні цитокіни, такі як — інтерлейкін (IL)-6, фактор некрозу пухлини (TNF)-α і сироватковий амілоїд А (Richette P., Funk-Brentano T., 2010).
За результатами останніх досліджень описана роль адипоцитокінів (або адипокінів) як медіаторів запалення (Bijlsma J.W.J. (Ed.), 2013). IL-6, який переважно синтезується у жировій тканині у пацієнтів із ожирінням, також може продукуватися жировою тканиною надколінка та підколінка всередині суглоба (Richette P. et al., 2011), що підтверджує зв’язок між ожирінням та розвитком ОА через системне запалення.
Ще одним із факторів ризику розвитку ОА є цукровий діабет і порушення толерантності до глюкози. Підвищення концентрації глюкози в суглобі призводить до зміни хрящової тканини, збільшуючи кількість кінцевих продуктів гліколізу, що, в свою чергу, активує вироблення хондроцитами і синовіоцитами продегратаційних і прозапальних медіаторів і змінює структуру субхондральної кістки. Також гіперглікемія викликає невелике системне запалення, що посилює ОА. У свою чергу, вплив гіперглікемії на нервову тканину, розвиток симетричної периферичної полінейропатії та стопи Шарко призводить до нервово-м’язової недостатності, м’язової слабкості, дестабілізації суглоба та виникнення вторинного ОА (Berenbaum Francis, 2011).
При дефіциті інсуліну, цукровому діабеті виникають порушення з боку сполучної тканини та судинної стінки — порушення обміну гіалуронової кислоти та хондроїтин сульфату, зменшення синтезу мукополісахаридів, що призводить до деградації хряща суглобів (Казимирко В.К. и соавт., 2006).
Останнє десятиліття також почали вивчати взаємозв’язок ОА з гіперурикемією. Підвищений рівень сечової кислоти у сироватці крові асоціювався з генералізованим ОА у людей, які перенесли ендопротезування кульшового суглоба (Sun Y. et al., 2000), тісний зв’язок також продемонстровано між тяжкістю ОА і рівнем сечової кислоти у синовіальній рідині у пацієнтів з гонартрозом і відсутністю в анамнезі подагри (Denoble A.E. et al., 2011), було опубліковано дані щодо поширеності підвищення рівня сечової кислоти у пацієнток з ОА (Ding X., Zeng C., 2016).
Існує думка, що ОА може бути пов’язаний з метаболічним синдромом або з кожним із його компонентів (Sellam J., Berenbaum F., 2013). Експериментальні дані свідчать про те, що цукровий діабет, дисліпідемія, АГ можуть бути незалежними факторами для розвитку ОА, навіть за відсутності ожиріння.
Підвищений рівень прозапальних медіаторів, зокрема IL-6 та -18, високо корелює з ожирінням, серцево-судинною патологією, нейродегенеративними захворюваннями і ОА (Howcroft T.K. et al., 2013). У пацієнтів з ішемічною хворобою серця спостерігається суттєве підвищення рівня IL-2, -4, -6 та -18 (прозапальних цитокінів, які беруть участь у деградації хряща), причому рівень IL-6 вищий у пацієнтів з інфарктом міокарда (Tedgui A., Mallat Z., 2006).
Призначення ефективної терапії у хворих на ОА завжди було складною проблемою. А скільки пацієнти із ОА зазвичай віком старше 40 років, а отже, мають не одне коморбідне захворювання, при їх лікуванні важливо враховувати вплив застосованих препаратів на показники пуринового, вуглеводного, ліпідного обмінів та можливість безпечного застосування в осіб із супутньою патологією.
На сьогодні медикаментозне лікування ОА проводять препаратами, які розподіляють на дві групи: модифікуючі симптоми захворювання (симптоматичні) — швидкодіючі й повільнодіючі (symptomatic slow acting drugs for osteoarthritis — SYSADOA) та модифікуючі хворобу (патогенетичні) (Алексеева Л.И., 2009). До першої групи належать симптоматичні препарати швидкої дії, а саме анальгетики та нестероїдні протизапальні препарати (НПЗП), здатні зменшувати інтенсивність болю, припухлість, скутість і покращувати функцію суглобів.
На сьогодні все більш значне місце в терапії при ОА займають симптоматичні препарати повільної дії (SYSАDOA). Проте дослідження цих препаратів та дискусія щодо їх застосування триває і нині (Яременко О.Б., 2014). Зміни поглядів західних фахівців можна зрозуміти зі змін рекомендацій з лікування остеоартрозу: 2003 р., EULAR (European League Against Rheumatism — Європейська антиревматична ліга (Jordan K.M. et al., 2003)): SYSАDOA показані всім хворим, вони полегшують симптоми і гальмують розвиток хвороби; 2007 р., EULAR: показані всім хворим, але вони лише полегшують симптоми; 2008 р., OARSI (Osteoarthritis Research Society International): показані лише тим, у кого вони виявили ефективність за 6 міс прийому, можливо, полегшують симптоми ОА; 2012 р., ACR (American College of Rheumatology): не рекомендуються при ОА і не полегшують симптоматику (Zhang W. 2005; 2007; 2010; McAlindon T.E. et al., 2014). На противагу цьому, в рекомендаціях ESCEO (The European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases — Європейська спільнота з клінічних та економічних аспектів остеопорозу та остеоартрозу) 2014 р. рецептурні препарати цієї групи були включені до алгоритму лікування при ОА (Bruyere O., 2014). А в 2016 р. підтверджена їх ефективність внаслідок вивчення результатів клінічних досліджень щодо впливу на симптоми та структуру ОА препаратів різних груп, в тому числі SYSАDOA (Sharma L., 2016).
Аналіз сучасної терапії при ОА послужив приводом для вивчення ефективності, впливу на біохімічні, прозапальні, імунологічні показники НПЗП та симптоматичних повільнодіючих протизапальних препаратів (SYSАDOA) у лікуванні пацієнтів із ОА, що і стало метою проведеного дослідження.
Мета дослідження — диференційний підхід до лікування пацієнтів із ОА залежно від наявності супутньої патології.
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
Досліджено 211 пацієнтів (172 жінки, 39 чоловіків) із ОА колінних суглобів I–ІІІ рентгенологічної стадії за Kellgren — Lawrence. Діагноз ОА встановлювали за критеріями ACR 1986 р. та EULAR 2010 р. перегляду. Всім пацієнтам проводили рентгенологічне дослідження колінних суглобів у прямій (передньозадній) і боковій проекції за допомогою стаціонарного рентгенівського апарата «Sirescop CX» (ВАТ «Київський завод реле та автоматики», Україна, 1999) в положенні стоячи без навантаження на досліджуваний суглоб при згинанні коліна на 30˚. Стадію ураження визначали за класифікацією J.H. Kellgren та J.S. Lawrence (1957).
Розподіл на 6 груп проведено залежно від лікування. Пацієнти 1-ї групи (n=30) приймали німесулід (Німесил®, «Берлін-Хемі АГ/Менаріні Груп») у дозі 100 мг двічі на добу, 2-ї групи (n=30) — мелоксикам (Моваліс®, «Boehringer Ingelheim») у дозі 15 мг 1 раз на добу протягом 14 днів. Пацієнти 3-ї групи (n=54) приймали діацереїн (Флекцерин, ПАТ «Київський вітамінний завод») у дозі 50 мг двічі на добу, а 4-ї групи (n=32) — хондроїтину сульфат-4,6 пташиного походження (Структум®, «Pierre Fabre Medicament») у дозі 500 мг двічі на добу протягом 6 міс. Пацієнти 5-ї групи (n=30) приймали глюкозаміну сульфат (Сінарта®, ПАТ «Фармак») у дозі 400 мг тричі на тиждень протягом 1,5 міс, 6-ї (n=35) — фітопрепарат стандартизованого екстракту кореня імбиру (Верта®, ТОВ «ОМНІФАРМА КИЇВ») у дозі 300 мг 2 рази на добу протягом 2 міс.
Оцінено динаміку загальноклінічних показників: збір скарг та анамнезу, об’єктивне обстеження, оцінювання артрологічного статусу хворих, анкетування (заповнення пацієнтами адаптованих опитувальників WOMAC, Лекена, візуальна аналогова шкала (ВАШ)), лабораторних — показників ліпідного (холестерин) та вуглеводного обміну (глюкоза крові), печінкові маркери (білірубін, аланінамінотрансфераза (АлАТ), аспартатамінотрансфераза (АсАТ)), креатинін, сечова кислота у крові, С-реактивний білок (СРБ). Імунологічні дослідження включали кількісне визначення в сироватці крові рівня IL-1β («Bender MedSystems GmbH», Австрія), TNF-α («Orgenium», Фінляндія), інсуліноподібного фактора росту (IGF)-1 («DRG», Німеччина), трансформуючого фактора росту (TGF)-β («DRG», Німеччина) імуноферментним методом. Облік реакції проводили на імуноферментному аналізаторі Lab-Line-100 («WestMedica», Австрія). Для аналізу стану обміну оксиду азоту (NО) вивчали вміст у крові обстежених хворих рівня нітритів як кінцевого продукту метаболізму NО за допомогою реактиву Гріса.
Відповідність розподілу даних клінічного дослідження закону нормального розподілу перевіряли тестом Колмогорова — Смирнова. Для опису даних використовували медіану та міжквартильний інтервал (Me, IQR), при нормальному розподілі середнє арифметичне значення і стандартну похибку (M±m), частоту та стандартну похибку (Р±m). Оскільки отримані в результаті клінічного дослідження дані мали відхилення від нормального розподілу варіаційного ряду, для порівняння груп нами використано непараметричні методи статистики — U-критерій Манна — Уїтні (для незалежних груп) та критерій Вілкоксона (для залежних груп). Для дослідження взаємозв’язку кількісних показників використовували кореляційний аналіз, знаходили критерій Спірмена (r), для якісних — використовували аналіз таблиць спряженості, знаходили критерій χ2, силу взаємозв’язку φ та відносний ризик (RR), 95% довірчий інтервал (CI). Застосовували програмно-математичний комплекс для персонального комп’ютера «Microsoft Exel 2007» (Microsoft) та комп’ютерні програми для статистичного аналізу та оброблення даних «STATISTICA® 6.0» (StatSoft Inc., США), «SPSS Statistics 20» (IBM, США).
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
У результаті дослідження у 211 обстежених серед супутньої патології діагностовано артеріальну гіпертензію у 94%, ішемічну хворобу серця — у 81% випадків. Відзначена висока частота сечокам’яної хвороби (СКХ) та мікронефролітіазу — 64%, що, можливо, пов’язано з наявністю гіперурикемії у більшості (62%) обстежених пацієнтів. Метаболічний синдром виявлено у 61,8% обстежених хворих. У 76% випадків відзначали поєднання декількох коморбідних захворювань.
Незважаючи на столітню історію застосування НПЗП, вони залишаються актуальними і незамінними завдяки унікальній комбінації їх протизапальної та знеболювальної дії. Особливо важливим є вибір НПЗП з урахуванням їх безпеки та впливу на хрящову тканину, а також на супутню патологію. Для цього на базі терапевтичного відділення Київської міської клінічної лікарні (КМКЛ) № 7 проведено дослідження щодо вивчення ефективності німесуліду та мелоксикаму.
На фоні проведеної терапії відзначено достовірне зменшення вираженості больового синдрому за ВАШ, при прийомі німесуліду — на 35,6%, при застосуванні мелоксикаму — на 13,34%. При оцінці альгофункціонального індексу Лекена виявлено статистично достовірне зменшення вираженості болю на 30,3% через 2 тиж прийому німесуліду, а у пацієнтів, які приймали мелоксикам, — на 25,7% через 2 тиж лікування (табл. 1).
| Показник | Німесулід | Мелоксикам | ||||||
|---|---|---|---|---|---|---|---|---|
| До лікування | Після лікування | До лікування | Після лікування | |||||
| Me | IQR | Me | IQR | Me | IQR | Me | Me | |
| ВАШ, мм | 57,5 | 53,5–65,5 | 35* | 31,25–42,25 | 60,00 | 57,00–67,00 | 55,00* | 57,5 |
| WOMAC, мм | ||||||||
| Біль | 193,00 | 117,5–340,25 | 91,00* | 48,75–160,75 | 342,50 | 51,75–434,75 | 197,00* | 26,25–261,50 |
| Скутість | 100,00 | 76,75–111,00 | 68,5* | 48,00–88,00 | 93,00 | 14,00–107,50 | 64,00* | 11,25–87,75 |
| Функціональна недостатність | 725,00 | 332,25–1167,75 | 414,00* | 166,25–734,00 | 646,00 | 64,00 | 436,50* | 44,25–577,00 |
| Індекс Лекена, балів | 9,5 | 8,00–12,75 | 6,5* | 5,25–9,00 | 11,00 | 8,00–14,00 | 8,00* | 6,00–11,00 |
| Імунологічні показники | ||||||||
| NO, мкмоль/л | 4,81 | 3,19–7,27 | 3,05* | 2,5–4,68 | 3,10 | 0,43–6,97 | 2,98 | 0,40–6,60 |
| CРБ, мг/л | 5,59 | 2,7–14,03 | 2,66* | 1,04–7,55 | 7,81 | 4,49–17,36 | 3,80* | 1,86–11,36 |
| IL-1B, пг/мл | 22,63 | 12,75–34,15 | 17,06* | 11,08–29,84 | 23,95 | 17,43–32,43 | 23,54 | 17,32–32,58 |
| IGF-1, нг/мл | 9,4 | 2,71–47,01 | 9,6 | 2,85–50,25 | 18,77 | 1,69–85,69 | 21,00 | 2,07–91,00 |
У табл. 1 і 2: *р<0,001 при використанні критерію Вілкоксона.
На фоні лікування німесулідом пацієнти відзначили підвищення фізичної активності та значне поліпшення рухового режиму, що знаходить відображення в достовірному зменшенні вираженості болю на 53,9%, скутості — на 29,7% і функціональних порушень — на 41,6%. У пацієнтів, які приймали мелоксикам, інтенсивність зменшення болю, скутості та функціональних порушень була менш вираженою: біль — на 37,3%, скутість — на 20%, функціональні порушення — на 26,6% через 2 тиж лікування (див. табл. 1).
При прийомі німесуліду виявлено статистично достовірне зниження рівня IL-1β на 14% (див. табл. 1), а також NO на 42,8%, на відміну від групи із застосуванням мелоксикаму, де ці показники не змінювалися. При застосуванні німесуліду виявлено зниження NO, основного індуктора запалення та деградації хрящової тканини при ОА, в той час як мелоксикам не впливав на рівень NO.
Циклооксигеназа (ЦОГ)-незалежні ефекти німесуліду насамперед полягають в інгібуванні активності NO-синтази і, відповідно, утворення NO і пероксинітриту (ОNOO–), які є ключовими медіаторами у процесі руйнування клітин організму й елементами запальної відповіді. Оскільки ОА виникає в осіб із супутньою кардіоваскулярною патологією, то такі особливості німесуліду, як активація синтезу інгібітора тканинного активатора плазміногену, блокування синтезу тромбоцитоактивуючого фактора, є надзвичайно важливими в запобіганні тромбоемболічним ускладненням (Lane N.E. et al., 2011).
Відзначено статистично достовірне зниження рівнів CРБ у плазмі крові — в групі німесуліду на 64,4%, у групі мелоксикаму — на 50,48%, що може свідчити про зменшення вираженості запальної відповіді в обох групах.
Результати аналізу даних біохімічних показників крові (білірубін, АлАТ, АсАТ, глюкоза, креатинін) свідчать про те, що при застосуванні обох препаратів статистично достовірних змін даних не виявлено (табл. 2). Проте відзначена тенденція до зниження рівня сечової кислоти з 375,33±24,6 до 321,57±19,6 мкмоль/л після застосування німесуліду, в той час як мелоксикам не впливав на її рівень, що може бути корисним при лікуванні пацієнтів із гіперурикемією.
| Показник | Німесулід | Мелоксикам | ||
|---|---|---|---|---|
| До лікування | Після лікування | До лікування | Після лікування | |
| Білірубін, мкмоль/л | 17,59±0,55 | 17,59±0,55 | 17,01±0,9 | 16,81±0,89 |
| АлАТ, мккат/л | 0,12±0,007 | 0,13±0,009 | 0,19±0,02 | 0,19±0,02 |
| АсАТ, мккат/л | 0,17±0,05 | 0,17±0,05 | 0,18±0,022 | 0,21±0,026 |
| Глюкоза, ммоль/л | 5,1±0,16 | 5,05±0,12 | 5,03±0,22 | 5,14±0,23 |
| Креатинін, мкмоль/л | 92,6±3,24 | 92,2±2,74 | 90,9±1,94 | 91,1±2,13 |
Результати аналізу застосування селективних НПЗП свідчать про достовірний клінічний ефект в обох групах, однак німесулід, на відміну від мелоксикаму, має більш виражений клінічний ефект, а саме: зменшення вираженості больового синдрому, скутості та функціональних порушень, що, можливо, пов’язано з його коротким механізмом дії (період напіввиведення (Т½) 3,2–6 год), в той час як мелоксикам має більш пролонгований механізм (Т½ становить 15–20 год). Крім того, німесулід може бути препаратом вибору при такій супутній патології, як серцево-судинні захворювання та гіперурикемія.
За останні роки ОА розглядається як запальний процес, в основі якого лежить продукція цитокінів, які запускають каскад запальної реакції, в результаті чого виникає пошкодження хрящової тканини. Серед симптоматичних протизапальних препаратів повільної дії (SYSАDOA) є препарат, який діє як інгібітор IL-1 та його патологічних ефектів — діацереїн. IL-1 є ключовим медіатором при ОА, він спричиняє пошкодження хряща за допомогою стимуляції продукції інших цитокінів, матриксних металопротеаз (ММП) і NO, викликає запальний процес при OA, апоптоз хондроцитів, активує остеокласти субхондральної кістки, що є причинами її змін, індукує синтез PG та зумовлює стійкий больовий синдром, стимулює власну продукцію, що забезпечує постійне пошкодження хряща.
Нами проведено дослідження щодо вивчення ефективності діацереїну у 54 хворих (49 жінок і 5 чоловіків) віком 30–75 років I–III рентгенологічної стадії за Kellgren — Lawrence.
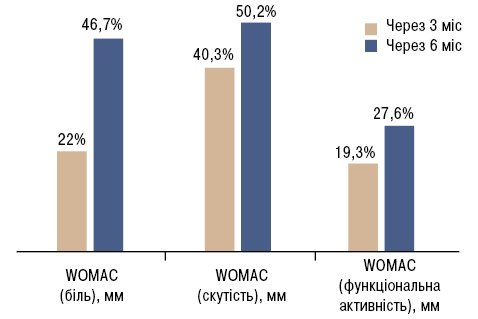
У результаті дослідження виявлено позитивний вплив діацереїну на динаміку показників суглобового синдрому, а саме статистично достовірне зниження вираженості болю за WOMAC на 46,7%, скутості — на 50,2%, покращення функціональної активності — на 27,6% (табл. 3, рис. 1).
| Показник | До лікування | Через 3 міс | Через 6 міс | |||
|---|---|---|---|---|---|---|
| Me | IQR | Me | IQR | Me | IQR | |
| WOMAC (біль), мм(0–500) | 238,00 | 217,25–287,75 | 186,00* | 125,00–202,25 | 130,50* | 98,00–168,50 |
| WOMAC (скутість), мм(0–200) | 114,00 | 92,00–134,25 | 68,00* | 55,50–76,00 | 56,50* | 46,00–68,00 |
| WOMAC (функціональна активність), мм(0–1700) | 765,50 | 612,00–902,75 | 617,00* | 528,00–692,00 | 578,00* | 437,00–643,50 |
| Сумарний індекс WOMAC(0–2400) | 1115,5 | 920,00–1312,25 | 852,00* | 721,75–969,25 | 750,00* | 657,50–858,00 |
У табл. 3, 10–17: *р<0,001, різниця вважається достовірною при р<0,05.
При застосуванні діацереїну отримано статистично достовірне зниження прозапальних цитокінів (TNF-α, IL-1), вільних радикалів, які беруть участь у деструкції хряща (NO), СРБ, а також статистично достовірне підвищення факторів росту (TGF-β, IGF-1). Отримані дані свідчать про високу клінічну ефективність, зменшення інтенсивності запального процесу та анаболічний ефект діацереїну у хворих на ОА (табл. 4).
| Показник | До лікування | Після лікування | р* | ||
|---|---|---|---|---|---|
| Me | IQR | Me | IQR | ||
| IL-1, пг/мл | 19,47 | 15,22–23,81 | 12,00 | 9,00–16,20 | 0,001 |
| NO, мкмоль/л | 4,09 | 3,00–4,19 | 2,20 | 1,00–3,44 | 0,001 |
| IGF-1,нг/мл | 38,00 | 22,00–57,50 | 98,00 | 77,00–119,25 | 0,001 |
| TNF-α, пг/мл | 22,31 | 17,33–29,30 | 11,20 | 8,70–14,70 | 0,001 |
| TGF-β, пг/мл | 25,96 | 11,66–43,58 | 109,11 | 97,47–163,87 | 0,001 |
У табл. 4–9: *різниця вважається достовірною при р<0,05.
Не відзначено динаміки лабораторних показників ліпідного обміну, білірубіну, печінкових маркерів, креатиніну та його кліренсу, що свідчить про можливість безпечного застосування препарату у пацієнтів із супутньою патологією, а статистично достовірне зниження рівня глюкози у крові — у пацієнтів із цукровим діабетом ІІ типу (табл. 5). Ці дані зіставні з іншим дослідженням 2011 р., в якому у пацієнтів із цукровим діабетом ІІ типу та ожирінням, які раніше не застосовували будь-яких діабетичних препаратів, виявлено, що застосування діацереїну підвищувало секрецію інсуліну та знижувало рівень глюкози крові (Ramos-Zavala M.G. et al., 2011), що, можливо, пов’язано зі зниженням прозапальних цитокінів (TNF-α та IL-1β), які беруть участь у апоптозі β-клітин підшлункової залози, що веде до зменшення секреції інсуліну з подальшим розвитком гіперглікемії. Згідно з отриманими нами даними, діацереїн здатний впливати на проанаболічні цитокіни, одним з яких є IGF-1, який є структурним аналогом інсуліну і має ряд спільних з ним властивостей, у проведеному нами дослідженні спостерігали статистично достовірне його підвищення, що, можливо, б





