
 Стаття
Стаття
 26.02.2025
26.02.2025
Отчет о проведении клинического исследования по изучению эффективности и переносимости препарата «Стифимол», производства ПАО «Киевский витаминный завод» Украина, у больных с гипертонической болезнью и ожирением
Е.И. Митченко ГУ Национальный научный центр "Институт кардиологии им. акад. Н.Д. Стражеско" НАМН Украины
РЕФЕРАТ
Ключевые слова: гипертоническая болезнь, ожирение, гарциния камбоджийская.
Отчет представлен на 31 стр., содержит 4 таблицы, 20 источников литературы.
Целью данного исследования является оценка эффективности и переносимости препарата «Стифимол», производства ПАО «Киевский витаминный завод», Украина, у больных с гипертонической болезнью и ожирением.
Задачи исследования:
- оценить эффективность исследуемого препарата у больных с гипертонической болезнью и ожирением, а также возможность его влияния на характеристики липидного и углеводного обменов.
- изучить переносимость и возможные побочные эффекты исследуемого препарата.
Исследование проводилось как открытое, контролируемое, рандомизированное и выполнялось в соответствии с требованиями, предъявляемыми Государственным Фармакологическим центром МЗ
Украины к клиническим испытаниям.
В исследование было включено 30 пациентов с гипертонической болезнью І-ІІ стадии 2 степени и ожирением І-ІІІ степени, которые находились на амбулаторном и/или стационарном лечении в отделе дислипидемий ГУ “ННЦ “Институт кардиологии им. Н. Д. Стражеско” НАМИ Украины. Все исследуемые в зависимости от состояния углеводного обмена составили 2 клинические группы: 1-я группа – 14 пациентов (средний возраст (55,1 ±2,9) лет) с гипертонической болезнью І-ІІ стадии 1-2 степени, ожирением ІІ -ІІІ степени и сахарным диабетом 2 типа (СД)). Во 2-ую группу вошли 16 больных (средний возраст (53,2 ±2,7) лет) с
гипертонической болезнью І—ІІ стадии 1-2 степени и ожирением І-ІІ степени без нарушения углеводного обмена. Hа протяжении 12 недель исследования больным не изменялась индивидуально подобранная антигипертензивная, гиполипидемическая и сахароснижающая терапия.
Схема лечения исследуемым препаратом: больным назначался препарат «Стифимол» в дозе 1 капсула 3 раза в день перед едой, запивая стаканом воды. Курс лечения для всех пациентов составил 2 месяца.
В результате исследования получены следующие результаты:
- Выявлено, что прием препарата «Стифимол» в дозе 1 капсула 3 раза в день на протяжении 8 недель у пациентов с ГБ, ожирением сопровождается уменьшением выраженности абдоминального ожирения и массы тела в среднем на 1,6 %, у пациентов с ГБ, ожирением и СД 2 типа на 3,6 %, что ассоциируется с оптимизацией углеводного и липидного обменов, показателей офисного АД.
- Обнаружено, что терапия препаратом «Стифимол» на протяжении 8 недель приема позволяет оптимизировать чувствительность периферических тканей к инсулину (снижение НОМА индекса с 5,3±0,7 до 4,4±0,8 ус. ед.) у пациентов с ГБ, ожирением и СД 2 типа, не ухудшая при этом данные характеристики у пациентов без нарушения углеводного обмена.
- Установлено, что снижение массы тела на фоне приема препарата «Стифимол» сочетается с оптимизацией эффективности стандартной антигипертензивной терапии и снижением ЧСС у пациентов всех групп, но более выраженная динамика снижения уровней САД на 8,9 % и ДАД на 11,2 % от исходного уровня отмечалась во 2-й группе пациентов без нарушения углеводного обмена.
- Выявлено, что терапия препаратом «Стифимол» на протяжении 8 недель приема позволяет оптимизировать эффективность стандартной гиполипидемической терапии, что ассоциировалось с тенденцией к снижению уровней общего ХС, ХС ЛПНП, ТГ у пациентов с ГБ и ожирением и достижением целевых уровней данных показателей в группе больных с ГБ, ожирением и СД 2 типа.
- Препарат «Стифимол» производства ПАО «Киевский витаминный завод», Украина продемонстрировал высокую безопасность и хорошую переносимость наряду с отсутствием побочных реакций у исследуемых пациентов.
ВВЕДЕНИЕ
За последнее десятилетие ожирение стало одним из самых быстро прогрессирующих хронических заболеваний в мире, распространенность которого приобрела характер неинфекционной эпидемии. Согласно данным ВОЗ, опубликованным в 2003г., около 1,7 млрд. человек на планете имели избыточную массу тела или ожирение. Средняя продолжительность жизни лиц с ожирением на 8-10 лет короче, чем у людей с нормальной массой тела. В конце 2010 года опубликованы данные анализа соотношений между индексом массы тела и смертностью от всех причин по данным ряда проспективных исследований, которые продемонстрировали, что у людей белой расы избыточный вес и ожирение ассоциируются с повышенной смертностью от всех причин. Избыточная масса тела в настоящее время рассматривается, как независимый фактор риска сердечно-сосудистых заболеваний, причем по своей значимости ожирение не уступает таким факторам риска, как повышенное артериальное давление (АД) или курение (1, 7). Ожирение тесно связано с другими факторами риска и влияет на выживаемость больных ИБС, способствует ранней инвалидизации населения и снижению, как общей продолжительности жизни, так и качества жизни вследствие развития сопутствующих заболеваний. Результаты исследования по изучению влияния ожирения на показатели смертности, в котором участвовало 4 576 785 мужчин и 588 369 женщин, продемонстрировали что повышенный индекс массы тела (ИМТ) был предиктором сердечно-¬сосудистой смертности, особенно у мужчин (относительный риск 2,9), а риск смертности от всех причин, включая сердечно-сосудистые заболевания и рак, прогрессивно повышался во всем диапазоне показателей ИМТ, соответствующих ожирению I-ІІІ степени у мужчин и женщин всех возрастных групп (9). Ожирение по характеру распределения жира подразделяется на абдоминальное, когда основная масса жира расположена в брюшной полости, на передней брюшной стенке, туловище, шее и лице (мужской или андроидный тип ожирения) и гиноидное, с преимущественным отложением жира на ягодицах и бедрах (женский тип ожирения). Нейрогормональные нарушения, сопутствующие абдоминальному ожирению, абдоминальная жировая ткань играют важную роль в развитии и прогрессировании ИР и связанных с ней метаболических расстройств. Повышенный уровень инсулина ведет к усилению процессов синтеза жиров и блокированию их распада. Увеличение количества жировых клеток сопровождается уменьшением плотности инсулиновых рецепторов на их поверхности и увеличением их инсулинорезистентности (ИР). При преимущественном отложении жира в висцеральной области, вследствие интенсивного липолиза высвобождаются свободные жирные кислоты (СЖК) в больших количествах и поступают в воротную вену и печень. Это приводит к уменьшению связывания гепатоцитами инсулина, его деградации и развитию ИР в печени, к торможению супрессивного действия инсулина на глюкогенез, а также к системной гиперинсулинемии, что способствует развитию периферической ИР (3). СЖК оказывают прямое токсическое воздействие на бета-клетки поджелудочной железы. При ИР и избытке СЖК нарушается обмен липидов и развивается атерогенная дислипидемия.
Абдоминальный тип ожирения является одним из важнейших факторов риска развития сахарного диабета 2 типа (СД) и выявляется у 90 % пациентов с данной патологией. Наличие абдоминального ожирения у мужчин, независимо от ИМТ, повышает риск развития СД в 3,5 раза, а у женщин с ОТ 92 см относительный риск в 5,1 раза больше по сравнению с женщинами с ОТ 67 см. По результатам 12-летнего наблюдения, включившего 43 457 женщин в возрасте от 40 до 64 лет, было показано что снижение массы тела на 5-10% (от 0,5 до 9,0 кг) сопровождалось уменьшением общей смертности на 20% и сердечно-сосудистой смертности на 9%. Уменьшение степени ожирения ассоциируется с оптимизацией уровня артериального давления (АД), что было продемонстрировано в ряде крупных многоцентровых исследований (16, 17). В одном из них, (TОMHS), снижение массы тела в результате активных профилактических мер через 18 мес. наблюдения составило в среднем 3,9 кг, что сопровождалось снижением диастолического АД (ДАД) на 2,3 мм рт. ст. и систолического АД (САД) на 2,9 мм рт. ст. (19). В исследовании ТАІМ, показано, что гипотензивный эффект снижения массы тела на 4,5 кг и более сравним с эффективностью назначения хлорталидона или атенолола (20). Существуют убедительные доказательства того, что уменьшение массы тела может предотвратить или замедлить развитие СД у лиц с ожирением. В Исследовании медицинских сестер (Nurses Health Study) у женщин, похудевших за 10 лет более чем на 5 кг, риск диабета снижался на 50% и более. Снижение степени ожирения ассоциируется с уменьшением выраженности дислипидемий, что было подтверждено результатами Шведского исследования (4). Так, у больных, похудевших на 2,4 кг и более за 1 год, было выявлено достоверное снижение концентрации триглицеридов, а у тех, кто похудел на 6,9 кг. и более — достоверное увеличение уровня холестерина ЛПВП.
Уменьшение массы тела па 5-10% от начальной величины сопровождается улучшением прогноза в отношении изменения характера кардиоваскулярного риска и снижения заболеваемости сахарным диабетом 2-го типа. Как известно, немедикаментозная терапия ожирения включает модификацию образа жизни и снижение калорийности суточного рациона, которые наиболее эффективно улучшают гликемический и липидный обмен. Так по данным российских ученых, применение редуцированных по калорийности рационов (1300-1700 калорий), в основном за счет олигосахаридов, с ограничением соли сопровождалось снижением избыточной массы тела, положительной динамикой показателей липидного профиля, нормализацией уровня инсулина и секреции катехоламинов. К сожалению, только менее половины пациентов с избыточной массой тела придерживаются необходимых диетических рекомендаций (6). В этой связи, использование медикаментозной терапии ожирения в первую очередь должно быть эффективным и безопасным у пациентов с кардиоваскулярными факторами риска. В последнее время значительной внимание привлекают комплексные натуральные препараты для лечения избыточной массы тела, содержащие растительные компоненты, способные эффективно снижать массу тела, не вызывая при этом побочных эффектов. К ним безусловно можно отнести отечественный препарат “Стифимол” производства ПАО «Киевский витаминный завод», 1 капсула которого содержит экстракта гарцинии камбоджийской (что соответствует содержанию кислоты гидроксилимонной 0,05 г) 0,1 г, хрома пиколината 0,0001 г, L-тирозина 0,5 г, левокарнитина (L-карнитина) 0,015 г, водорослей бурых сухого экстракта (Fucus vesiculosus L.), в пересчете на йод 0,037 мг. Гарциния камбоджийская является одним из основных растительных источников гидроксилимонной кислоты (ГЛК), которая обеспечивает эффективный механизм физиологического снижения массы тела за счет снижения активности фермента цитратлидазы, что в свою очередь подавляет образование ацетил-КоА и ограничивает дальнейший синтез жирных кислот через малонил-КоА (5, 15). В то же время под действием ГЛК происходит активация фермента карнитинацилтрансферазы, благодаря чему активируется образование карнитина и, соответственно, усиливается транспорт внутриклеточных жирных кислот в митохондриях и их окисление. Регулирующее влияние ГЛК на аппетит заключается в ее опосредованном влиянии на активность нейронов гипоталамуса, отвечающих за чувство голода и сытости. Блокируя образование жирных кислот из углеводов, ГЛК приводит к повышению гликогена в печени, что поддерживает необходимую концентрацию глюкозы, при которой нейроны гипоталамуса не стимулируют аппетит (3, 18). В некоторых исследованиях было показано, что на фоне приема ГЛК отмечалось уменьшение массы тела в среднем на 5 кг за 2 месяца, снижение уровня холестерина на 14% больше, чем в контрольной группе, при этом характерной особенностью было отсутствие у пациентов желания употреблять продукты, содержащие большое количество легкоусваиваемых углеводов. Также в эксперименте было изучено влияние экстракта (1г/кг веса) Гарцинии камбоджийской на липидный обмен. У крыс альбиносов получавших этанол в течение 45 дней было отмечено отсутствие постпрандиального повышения уровней липидов в сыворотке крови и снижение перекисного окисления липидов с образованием свободных радикалов (8, 11, 12). В исследованиях последних лет была продемонстрирована дополнительная терапевтическая эффективность ГКЛ. Японскими учеными в эксперименте на животных была показана возможность ускорять метаболизм углеводов и жиров, как в покое, так и при физических нагрузках. Влияние на обмен инсулина гарцинии камбоджийской изучался в эксперименте японскими учеными: уровни инсулина в сыворотке подопытных мышей пролеченных 3,3% экстрактом данного растения в течение 4 недель были ниже, чем в группе контроля. В эксперименте на мышах, для изучения острого токсического действия при внутрижелудочном введении использовались три дозы препарата (терапевтическая – 100 мг/кг; 5 и 10- кратная терапевтической) (10, 13). Установлено, что по параметрам острой токсичности при внутрижелудочном введении мышам и крысам препарат «Стифимол» относится к V классу токсичности (практически нетоксичные вещества). Физиологические, гематологические, биохимические и гистоморфологические показатели подопытных животных не отличались от таковых у интактных животных и не выходили за пределы физиологической нормы для данного вида (14).
Другим важным составляющим препарата, способным оказывать влияние на показатели массы тела, является ароматическая альфа – аминокислота тирозин, которая представлена оптической изомерной L формой. L-Тирозин – заменимая аминокислота, которая образуется из фенилаланина и входит в состав почти всех белков, в частности пепсина и инсулина. Из тирозина в организме синтезируется ряд важных веществ: тирамин и 3,4-дигидроксифенилаланин – предшественники катехоламинов, а также дийодтирозин, из которого образуется тироксин. Тирозин является предшественником нейромедиаторов норадреналина и дофамина. Эта аминокислота участвует в регуляции настроения; недостаток тирозина приводит к дефициту норадреналина, что, в свою очередь, приводит к депрессии. Тирозин, подавляя аппетит, способствует уменьшению количества адипозной ткани, инициирует выработку мелатонина и улучшение функции надпочечников, щитовидной железы и гипофиза (2).
Таким образом, появление на фармацевтическом рынке Украины отечественного препарата «Стифимол» производства ПАО «Киевский витаминный завод», содержащего натуральные растительные компоненты для эффективного снижения массы тела, является актуальным и необходимым.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследование было включено 30 пациентов с гипертонической болезнью І-ІІ стадии 2 степени и ожирением І-ІІІ степени, которые находились на амбулаторном и/или стационарном лечении в отделе дислипидемий ГУ “ННЦ “Институт кардиологии им. Н. Д. Стражеско” НАМН Украины. Все исследуемые, в зависимости от состояния углеводного обмена, составили 2 клинические группы: 1-я группа – 14 пациентов (средний возраст (55,1 ±2,9) лет) с гипертонической болезнью І-ІІ стадии 1-2 степени, ожирением ІІ-ІІІ ст. и сахарным диабетом 2 типа (СД). Во 2-ую группу вошли 16 больных (средний возраст (53,2 ±2,7) лет) с гипертонической болезнью І-ІІ стадии 1-2 степени и ожирением І-ІІ ст. без нарушения углеводного обмена. На протяжении 12 недель исследования всем больным не изменялась индивидуально подобранная антигипертензивная, гиполипидемическая и сахароснижающая терапия.
Диагноз артериальной гипертензии выставлялся согласно рекомендациям Украинской ассоциации кардиологов 2008 г. АГ у всех исследуемых больных соответствовала I и II степени (мягкая и умеренная АГ).
Определение степени ожирения проводилась в соответствии с рекомендациями ВООЗ (1997 г.) с расчетом ИМТ по формуле: ИМТ = масса тела /рост2 [кг/м2]
Избыточная масса тела определялась при ИМТ от 25 до 29,9 кг/м2, ожирение (Ож.) I ст. – при ИМТ от 30,0 до 34,9 кг/м2, ожирение II и III ст., определялись при значениях этого показателя от 35,0 до 39,9 кг/м2 и более 40 кг/м2 соответственно. Абдоминальное ожирение верифицировалось при окружности талии у мужчин > 94 см, у женщин > 88 см.
Критерии включения:
- мужчины и женщины в возрасте от 30 до 70 лет;
- установленные диагнозы:
- Гипертоническая болезнь I – II степени;
- Избыточная масса тела и ожирение I – III.
- способность пациента к адекватному сотрудничеству в процессе исследования.
Критерии исключения:
- повышенная чувствительность к компонентам препарата, в том числе к йоду;
- беременность, лактация;
- острые состояния (инфекции, травмы, операции) в период менее 2-х месяцев до начала исследования;
- нарушение функции щитовидной железы;
- любые сопутствующие декомпенсированные заболевания или острые состояния, наличие которых способно существенно повлиять на результаты исследования;
- клинически значимые отклонения лабораторных показателей, требующие дополнительного обследования и интерпретации данных;
- участие в любом другом клиническом испытании.
- Исследование должно было бы быть досрочно прервано в случае:
- возникновения серьезных побочных реакций у большинства пациентов в первые дни или часы испытания;
- обоснованного решения Заказчика о прерывании испытания;
- грубых нарушений протокола или этических норм проведения клинических испытаний, выявленных в результате инспекционных проверок
Методы исследования включали: определение роста и веса пациента с дальнейшим расчетом ИМТ, определение окружности талии (ОТ), измерение офисного АД, определение основных биохимических показателей сыворотки крови натощак (АЛТ, ACT, КФК, креатинина, глюкозы, инсулина), а так же общего холестерина (ХС), триглицеридов (ТГ), холестерина липопротеинов высокой плотности (ХС ЛПВП), холестерина липопротеинов очень низкой плотности (ЛПОНП), холестерина липопротеинов низкой плотности (ХС ЛПНП), коэффициента атерогенности плазмы. Проводился иммуноферментный анализ количественного определения инсулина в плазме крови человека с помощью набора DRG®Insmkin с последующей оценкой чувствительности тканей к инсулину с помощью НОМА индекса. Данный показатель рассчитывали по формуле: уровень инсулина натощак (МЕд/мл) х глюкоза крови натощак (ммоль/л)/22,5. При НОМА индексе выше 3 усл.ед. диагностировали ИР. Всем пациентам были даны рекомендации по модификации образа жизни и соблюдению диеты с ограничением жиров животного происхождения.
Схема лечения исследуемым препаратом: больным назначался препарат «Стифимол» в дозе 1 капсула 3 раза в день перед едой, запивая стаканом воды. Курс лечения для всех пациентов составил 8 недель.
После 4-х недель приема препарата проводилось повторное обследование пациента с определением динамики массы тела, офисного артериального давления, оценкой переносимости препарата и анализом возможных побочных реакций.
Курс лечения для всех пациентов составил 8 недель. В конце исследования всем пациентам проводилось повторное определение всех антропометрических, биохимических параметров, измерение АД, анализ приверженности к терапии и переносимости препарата.
В качестве базисной терапии все испытуемые получали лечение с использованием подобранной комбинации препаратов (антагонисты кальция, ингибиторы АПФ, аспирин, диуретики, статины). Базисная гипогликемическая терапия у пациентов с СД в течение исследования не изменялась.
Оценка переносимости проводилась на основании
- Объективных данных, полученных исследователем в ходе проведения исследования.
- Данных лабораторного обследования, производимого до начала и по завершении курса лечения исследуемым препаратом.
- Субъективных ощущений, сообщаемых пациентом.
Таблица 1. Шкала переносимости препарата
Статистическая обработка полученных результатов проводилась с использованием статистических пакетов Statistica ver.5.5 и SPSS ver. 10.5.
РЕЗУЛЬТАТЫ
Было выявлено, что пациенты 1 группы в начале исследования имели наибольшие проявления абдоминального ожирения и значения ИМТ, которые соответствовали ожирению II и III степени, по сравнению со 2 группой. Показатели углеводного обмена свидетельствовали об относительной компенсации СД у больных 1 группы (HbAlc 6,7±0,4%). На фоне терапии препаратом «Стифимол» в течение 2 месяцев было отмечено уменьшение окружности талии (ОТ) и ИМТ у всех пациентов. Наиболее динамичное снижение массы тела было отмечено у пациентов 1 группы с ГБ, ОЖ и СД, изначально имевших наиболее выраженные проявления ожирения (ИМТ 39,1±1,9 кг/м2). ИМТ уменьшился на 5,6%, в то время как во 2 группе изменение данного показателя составило – 3,8%. (табл.2). Данные изменения ассоциировались с оптимизацией показателей углеводного обмена, а именно, уменьшением показателей тощаковой гликемии с 7,6±0,4 до 6,8±0,5 ммоль/л и HbAlc с 6,7±0,4 до 6,2±0,2%, а также улучшением чувствительности периферических тканей к инсулину по данным НОМА индекса. В то же время изначально нормативные показатели углеводного обмена во 2 группе оставались без отрицательной динамики на фоне терапии исследуемым препаратом.
Таблица 2. Динамика антропометрических данных и показателей углеводного обмена у исследуемых больных.
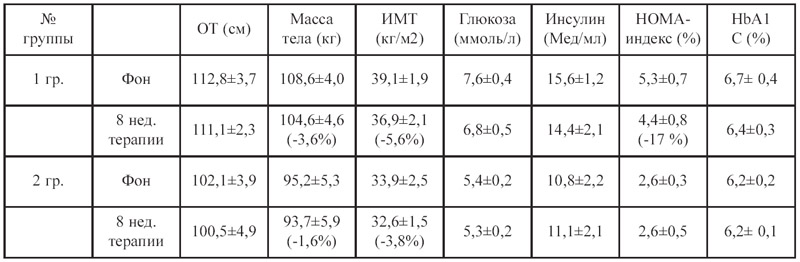
Хорошо известным является факт взаимосвязи между снижением избыточной массы тела и нормализацией уровней АД (класс I, уровень доказательства А). Происходит это во многом благодаря гемодинамическим и нейрогуморальным факторам. Уменьшение степени ожирения ассоциируется со снижением сердечного выброса, периферического сосудистого сопротивления, замедлением частоты сердечных сокращений. С другой стороны отмечается снижение уровней норадреналина и альдостерона плазмы, активности ренина и ангиотензинпревращающего фермента. Наши данные продемонстрировали, что в конце наблюдения у пациентов 1 и 2 групп отмечались тенденции к снижению офисного как систолического АД (с 149,1±3,3 до 141,4±3,1 и с 145,9±3,4 до 132,8±3,8 мм. рт. ст.), так и диастолического АД (с 95,5±2,1 до 91,7±2,5 и с 92,1±2,1 до 81,8±2,9 мм. рт. ст.) соответственно. Данные изменения сопровождались снижением частоты сердечных сокращений (ЧСС) в обеих группах (табл.3).
Таблица 3. Показатели офисного АД у исследуемых пациентов
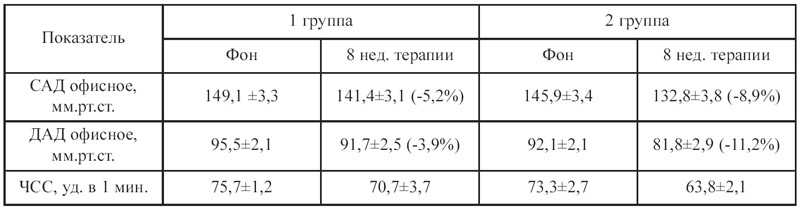
Таким образом, снижение массы тела сочетается с оптимизацией углеводного обмена у пациентов с СД, дополнительным антигипертензивным эффектом у пациентов всех исследуемых групп, но в большей степени положительная динамика отмечалась во 2 группе пациентов без нарушения углеводного обмена.
Анализ показателей липидограммы продемонстрировал в исходе отсутствие целевых значений общего холестерина (ХС), холестерина липопротеинов низкой плотности (ХС ЛПНП) у пациентов обеих групп, несмотря на прием статинов до начала исследования. На фоне приема препарата «Стифимол» продемонстрировано снижение данных показателей в обеих группах, причем в первой, наиболее тяжелой в клиническом плане группе, удалось достичь целевых значений общего ХС и ХС ЛПНП (4,0±0,3 и 1,9±0,2 ммоль/л соответственно), также у данного контингента больных отмечалась тенденция к нормализации уровня триглицеридов.
Таблица 4. Динамика антропометрических данных и показателей липидного обмена у исследуемых больных.
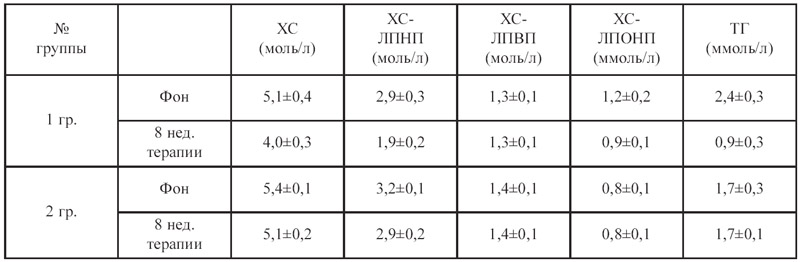
Наши результаты подтверждают литературные данные о возможности Гарцинии камбоджийской оптимизировать показатели липидного обмена за счет снижения перекисного окисления липидов, что было доказано в эксперименте японскими учеными (8).
Таким образом, в настоящее время пандемия ожирения является неизбежным следствием того, что большая часть населения оказалась в условиях, благоприятствующих малоподвижному образу жизни и избыточному поступлению калорий с пищей. Во всех регионах мира прогнозируется дальнейший рост числа тучных людей и предполагается, что к 2025 г. ожирением будут страдать 40% мужчин и 50% женщин. С распространением ожирения увеличиваются ассоциированные с ним тяжелые соматические заболевания: сахарный диабет 2-го типа, артериальная гипертензия, ИБС, атеросклероз, онкологическая патология и др. Медикаментозная терапия ожирения является составным элементом комплексной программы по снижению массы тела, включающей соблюдение диетических рекомендаций, физическую активность, модификацию образа жизни, в связи с чем использование безопасных и эффективных лекарственных препаратов для лечения пациентов с избыточной массой тела является приоритетной задачей. Важно отметить, что зарегистрированное в Украине лекарственное средство «Стифимол» приводит к стойкому клинически значимому уменьшению индекса массы тела, что ассоциируется с оптимизацией углеводного и липидного обменов, повышением эффективности стандартной антигипертензивной и гиполипидемической терапии, характеризуется благоприятным соотношением польза/риск и является эффективной составляющей в комплексной терапии больных с ожирением и связанных с ним кардиометаболических осложнений.
За время проведения исследования, терапия препаратом «Стифимол» производства ПАО «Киевский витаминный завод», Украина в дозе 1 капсула три раза в сутки на протяжении 8 недель приема хорошо переносилась пациентами при отсутствии побочных эффектов и динамики ферментов крови. Через 1 месяц после завершения приема препарата «Стифимол» у пациентов обеих групп сохранялись достигнутые позитивные тенденции в показателях углеводного и липидного обменов.
ВЫВОДЫ
1. Выявлено, что прием препарата «Стифимол» в дозе 1 капсула 3 раза в день на протяжении 8 недель у пациентов с ГБ, ожирением сопровождается уменьшением выраженности абдоминального ожирения и массы тела в среднем на 1,6%, у пациентов с ГБ, ожирением и СД 2 типа на 3,6 %, что ассоциируется с оптимизацией углеводного и липидного обменов, показателей офисного АД.
2. Обнаружено, что терапия препаратом «Стифимол» на протяжении 8 недель приема позволяет оптимизировать чувствительность периферических тканей к инсулину (снижение НОМА индекса с 5,3±0,7 до 4,4±0,8 ус. ед.) у пациентов с ГБ, ожирением и СД 2 типа, не ухудшая при этом данные характеристики у пациентов без нарушения углеводного обмена.
3. Установлено, что снижение массы тела на фоне приема препарата «Стифимол» сочетается с оптимизацией эффективности стандартной антигипертензивной терапии и снижением ЧСС у пациентов всех групп, но более выраженная динамика снижения уровней САД на 8,9% и ДАД на 11,2% от исходного уровня отмечалась во 2-й группе пациентов без нарушения углеводного обмена.
4. Выявлено, что терапия препаратом «Стифимол» на протяжении 8 недель приема позволяет оптимизировать эффективность стандартной гиполипидемической терапии, что ассоциировалось с тенденцией к снижению уровней общего ХС, ХС ЛПНП, ТГ у пациентов с ГБ и ожирением и достижением целевых уровней данных показателей в группе больных с ГБ, ожирением и СД 2 типа.
5. Препарат «Стифимол» производства ПАО «Киевский витаминный завод», Украина продемонстрировал высокую безопасность и хорошую переносимость наряду с отсутствием побочных реакций у исследуемых пациентов.
ЛИТЕРАТУРА
- Біловол О.М, Ковалева О.М Ожиріння в практиці кардіолога та ендокринолога. Тернопіль ТДМУ «Укрмедкнига» 2009 р. Стор.391
- Е.С. Северина. Биохимия, — М.,2003.
- Ройтберг Г.Е. Метаболический синдром. Москва. «МЕДпресс- информ». Стр. 160- 176
- Berger W. Comparison of guar gum, wheat bran and placebo on carbohydrate and lipid metabolism in type II diabetics. Schweiz Меd Wochenschr. 1990 Mar 24; 120(12):402-8.
- Chatterjee, A., Bagchi, D. & Stohs, S.J. (2004) Physico-chemical properties of a novel (-)-hydroxусіtric acid extract and its effect on body weight, selected organ weights, hepatic lipid peroxidation and DNA fragmentation, hematology and clinical chemistry, and histopathological changes over a period of 90 days. Molec. Cell Biochem., 260(1 -2), 171-186
- D.De Bacquer, G.De Backer. EUROASPIRE III: Lifestyle and risk factor management and use of drug therapies in coronary patients from 22 countries in Europe. European Journal of Cardiovascular Nursing , Volume 7 , Pages S28 – S28, 2008
- European Guidelines on cardiovascular disease prevention in clinical practice (version 2012) The Fifth Joint Task Force оf the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice. European Heart Journal. doi:10.1093/eurheartj/ehs092.
- Hayamizu K., Hirakawa H., Oikawa D., Nakanishi T., Takagi Т., Tachibana, T. & Furuse, M. (2003) Effect of Garcinia cambogia extract on serumleptin and insulin inmice. Fitoterapia, 74, 267-273
- National Heart, Lung, and Blood Institute Obesity Education Initiative. Clinical guidelines on the identification, evaluation, and treatment, of overweight and obesity in adults; the evidence report. Bethesda, MD: US Department of Health and Human Services, 1998
- Loe, Y.C., Bergeron, N„ Rodriguez, N. & Schwarz, J.-M. (2001) Gas chromatography/mass spectrometry method to quantify blood hydroxycitrate concentration. Analytical Biochemistry, 292, 148-154
- Mahendran, P. & Shyamala Devi, C.S. (2001) The modulating effect of Garcinia cambogia extract on ethanol-induced peroxidative damage in rats. Indian Journal of Pharmacology, 33, 87-91
- Mahendran, P., Sabitha, K.E. & Shyamala Devi, C.S. (2002) Prevention ofHCl-ethanol induced gastric mucosal injury in rats by Garcinia cambogia extract and its possible mechanism of action. Indian J. Exper. Biol., 40, 58-62
- Mattes, R.D. & Bormann, L. Effects of(-)-hydroxycitric acid on appetite variables. Physiol. 2000, Behav., 71, 87-9414 Ohia, S.E., Olubusayo Awe, S., LeOay, A.M., Opere, C.A. & Bagehi, D.
- (2001) Effect of hydroxycitric acid on serotonin release from isolated rat brain cortex. Res. Commun. Molec. Pathol. Pharmacol., 109(3&4), 210-216
- Ohia, S.E., Opere, C.A„ LeDay, A.M., Bagchi, M„ Bagchi, D., Stohs, SJ. (2002)
- Safety and mechanismof appetite suppression by a novel hydroxycitric acid extract (HCA-SX). Molecular and Cellular Biochemistry, 238, 89-103
- S. Rasmussen, J. Jeppesen, Tine W. Hansen. Insulin Resistance, the Metabolic Syndrome, and Risk of Incident CVD: Results. J Am Coll Cardiol. 2007; 49 (21):2112-2119
- Rutter Ketal. Insulin Resistance, the Metabolic Syndrome, and Incident Cardiovascular Events in the Framingham Offspring Study. Diabetes, november 2005, vol.54 3250-3257
- Soni, M.G., Burdock, G.A., Preuss, H.G., Stohs, S .J., Ohia, S.E. & Bagchi, D. (2004) Safety assessment of (-)-hydroxycitric acidand Super CitriMax, a novel calcium/potassium salt. Food Chem. Toxicol., 42(9), 1513-1529
- Schnaper H, Schoenberger J. Characteristics of participants at baseline in the Treatment of Mild Hypertension Study (TOMHS). Am J Cardiol. 1990 Sep 25;66(9):32C-35C
- Wassertheil-Srnoller S, Oberman A. The Trial Of Antihypertensive Interventions and Management (TAIM) Study. Final results with regard to blood pressure, cardiovascular risk, and quality of life. Am J Hypertens. 1992 Jan;5(1):37-44
Стаття надана мовою оригіналу






