
 Статья
Статья
 28.01.2025
28.01.2025
Вплив комбінації Антралю та Артіхолу на концентрацію циркулюючих імунних комплексів та їхній молекулярний склад у крові хворих на хронічний некалькульозний холецистит, поєднаний з хронічним вірусним гепатитом С мінімального ступеню активності
Соцька Я.А. Луганський державний медичний університет
Вступ
На тлі зростання за останні десятиріччя в Україні, як і в інших країнах СНД захворюваності на хронічну патологію печінки та жовчного міхура (ЖМ) [8], все більше привертає до себе увагу спеціалістів та практичних лікарів проблема сполученої патології, яка охоплює водночас два та більше органа або навіть функціональні системи організму [5]. Відомо, запальні процеси у ЖМ у вигляді хронічного некалькульозного холециститу (ХНХ) як правило, сполучаються з хронічними дифузними ураженнями печінки, зокрема з хронічними вірусними гепатитами С (ХВГС), при цьому, за даними наших досліджень, при наявності такої коморбідної патології гепатобіліарної системи (ГБС), в клінічній картині сполученої хвороби нерідко на перший план виступає саме симптоматика загострень хронічного запального процесу у ЖМ, у той час як ХВГС може мати низький або навіть мінімальний ступінь активності (МСА) [4, 7, 9, 10].
В теперішній час все більшу увагу привертає можливість використання засобів фітотерапії з метою лікування та медичної реабілітації хворих з хронічною патологією внутрішніх органів, в тому числі ураженнями ЖМ та печінки [3, 14, 16]. При цьому серед фітопрепаратів, які використовують при лікуванні патології ГБС, суттєве місце належить лікарським засобам з артішоку польового (колючого), тобто Сynara scolymus L. [3, 9]. В цьому плані перспективним є також використання комбінацій препаратів з артішоку колючого та сучасних гепатопротекторів з різноманітними механізмами фармакологічної дії [10, 14]. В наших попередніх роботах досить переконливо доведена ефективність застосування препаратів артішоку в комбінації з вітчизняним гепатозахисним засобом антралем в комплексі медичної раебілітації хворих на ХНХ, сполучений з ХВГС з МСА [10]. При детальному вивченні патогенезу захворювань гепатобіліарної локалізації з’ясовано, що значна роль у розвитку та прогресуванні патології печінки та ЖМ належить імунній системі організму людини [7, 13]. При патологічних зсувах імунного гомеостазу у хворих з’являється синдром імунотоксикозу різного ступеня вираженості, про який можна судити за рівнем циркулюючих імунних комплексів (ЦІК), особливо найбільш патогенних їх фракцій (середньомолекулярної та дрібномолекулярної) [12]. Тому можна було вважати доцільним та перспективним проаналізувати вплив комбінації препарату рослинного походження з артішоку колючого — артіхолу [2] та гепатопротектору антралю [1] на концентрацію циркулюючих імунних комплексів та їхній молекулярний склад у крові пацієнтів з коморбідною патологією ГБС у вигляді ХНХ, сполученого з ХВГС з МСА.
Зв’язок роботи з науковими програмами, планами, темами. Робота виконана відповідно до основного плану науково-дослідних робіт (НДР) Луганського державного медичного університету і являє собою фрагмент теми НДР: «Клініко-патогенетична характеристика коморбідної патології: хронічного некалькульозного холециститу, поєднаного з хронічним вірусним гепатитом С мінімального ступеня активності на тлі вторинних імунодефіцитних станів, лікування та медична реабілітація» (№ держреєстрації 0108U004716) та «Ефективність фітопрепаратів та засобів рослинного походження в лікуванні та медичній реабілітації хворих з патологією системи травлення та вторинними імунодефіцитними станами» (№ держреєстрації 0108U009463).
Метою роботи було вивчення впливу комбінації гепатопротектору антралю та препарату рослинного походження артіхолу на концентрацію ЦІК та їхній молекулярний склад у крові хворих на ХНХ, поєднаний з ХВГС з МСА в періоді медичної реабілітації.
Матеріали та методи дослідження
Під наглядом знаходилося дві групи хворих на ХНХ, сполучений з ХВГС з МСА: основна (62 особи), яка отримувала в комплексі медичної реабілітації комбінацію антралю та артіхолу, і група зіставлення (68 особи), яка одержувала загальноприйняту медикаментозну терапію. Серед обстежених було 28+31 чоловіків та 34+37 жінок; вік хворих складав від 18 до 59 років. Обидві групи хворих, які знаходилися під наглядом, були рандомізовані за віком, статтю, тривалистю перебігу ХНХ і ХВГС, частотою загострень патологічного процесу в ЖМ і печінці протягом останнього календарного року. Діагноз патології ГБС встановлювався експертним шляхом з урахуванням даних анамнезу, результатів клінічного та лабораторного (біохімічного) обстеження, яке характеризувало функціональний стан печінки, а також даних сонографічного дослідження органів черевної порожнини. В усіх обстежених хворих вірусна етіологія хронічного ураження печінки була встановлена за допомогою імуноферментного аналізу (ІФА) крові на наявність маркерів вірусу гепатиту С (HCV) та потім підтверджена методом ланцюгової полімеразної реакції.
При цьому до роботи включали лише хворих з наявністю помірного загострення хронічного запального процесу у ЖМ та при низькому ступеню активності ХВГС, що характеризувалося помірним цитолізом (активність АлАТ не перевищувала 2,0 ммоль/лхгод та активність АсАТ була не вище 1,4 ммоль/лхгод) при вірусному навантаженні не більше 300 тис/мл копій РНК HCV. При проведенні генотипування HCV було встановлено, що основним генотипом вірусу гепатиту С був перший (1), який виявлений у 87 особи (66,92%), зокрема у 43 пацієнтів (33,08%) — генотип 1b. Генотип 2 HCVбув виявлений у 11 хворих (8,5%), генотип 3 HCV — у 23 хворих (17,69%). У 9 пацієнтів (6,89%) генотип HCVвстановлений не був.
Обсяг біохімічного обстеження включав визначення рівня загального білірубіну та його фракцій (вільної та зв’язаної), активності сироваткових амінотрансфераз (АлАТ, АсАТ) з вирахуванням коефіцієнту де Рітіса (АсАТ/АлАТ), екскреторних ферментів (лужної фосфатази — ЛФ та гамаглутамілтранспептидази — ГГТП), показника тимолової проби, вмісту холестерину та Р-ліпопротеїдів у сироватці, загального білка та білкових фракцій, цукру крові, протромбінового індексу уніфікованими методами. Визначалась також загальна активність лактатдегідрогенази (ЛДГ) та її ізоферментний спектр методом електрофорезу в агарозному гелі за допомогою пристрою ПЕФ-3 в камері горизонтального електрофорезу.
У комплексі імунологічного дослідження у всіх хворих визначали концентрацію ЦІК у сироватці крові методом преципітації в розчині поліетиленгліколя (ПЕГ) з молекулярною масою 6000 дальтон [11]. Молекулярний склад ЦІК з виділенням фракцій велико- (>19S), середньо- (11S–19S) та дрібномолекулярних (<11S) імунних комплексів визначали шляхом диференційованої преципітації у 2,0%, 3,5% та 6% розчинах ПЕГ [11, 12]. Враховували, що за рівнем ЦІК, особливо найбільш патогенних (середньомолекулярної та дрібномолекулярної) їх фракцій, можна судити про вираження синдрому імунотоксикозу [12].
Хворі обох груп отримували підтримуючу інтерферонотерапію лаферобіоном по 1 млн МО в ректальних свічках 2 рази на тиждень та індуктор синтезу ендогенного інтерферону — циклоферон по 150 мг (1 таблетці) внутрішньо 2 рази на тиждень, антиоксиданти (аскорбінову кислоту, токоферолу ацетат або аєвіт), ентеросорбенти (полісорб, ентеросгель). Крім того, пацієнти основної групи додатково в комплексі медичної реабілітації отримували гепатопротектор антраль по 0,2 г (1 таблетці) 3 рази на добу усередину протягом 25–30 діб поспіль в залежності від досягнутого ефекту та препарат рослинного походження артіхол усередину по 0,4 г (2 таблетки) 3 рази на добу безпосередньо після вживання їжі протягом такого ж періоду. Антраль є сучасним гепатопротектором, що володіє вираженою антиоксидантною дією, зокрема підтримує активність системи АОЗ, обумовлює стабілізацію мембран гепатоцитів [15]. Одночасно цьому препарату властиві імуномодулююча, протизапальна та противірусна активність [1]. Антраль не спричиняє алергічної та імунотоксичної дії. Цей лікарський засіб виробляється в Україні ОАО «Фармак» та зареєстрований 17.08.2007 р. Наказом МОЗ України № 483 (№ реєстраційного посвідчення UA/6893/01/01). Артіхол — це препаратрослинного походження, фармакологічні властивості якого обумовлені фізиологічно активними речовинами, що входять до складу артішоку польового (колючого) [2]. Він володіє жовчогінною (холеретичною і холекінетичною), гепатопротекторною, антиоксидантною, мембраностабілізуючою і детоксикуючою діями [3]. Цей лікарський засіб нормалізує процеси жовчоутворення і жовчовиділення, здійснює дезінтоксикаційну дію, володіє гіпохолестеринемічним ефектом, через поліпшення клубочкової фільтрації нирок сприяє виведенню з організму сечовини, креатиніну, а також різних токсичних речовин [3, 9]. Артіхол випускається вітчизняною фармацевтичною компанією ЗАТ «Київський вітамінний завод» та зареєстрований в Україні 16.11.2006 р. Наказом МОЗ України № 758 (№ реєстраційного посвідчення UA/5383/01/01) [2].
Статистичну обробку отриманих результатів дослідження здійснювали на персональному комп’ютері IntelPentiumIII 800 за допомогою одно- і багатофакторного дисперсійного аналізу (пакети ліцензійних програм Microsoft Office 97, Microsoft Exel Stadia 6.1/prof та Statistica), враховуючи при цьому основні принципи застосування статистичних методів у клінічних дослідженнях [6].
Отримані результати та їх обговорення
Протягом диспансерного спостереження у низки хворих виявлялися клініко-лабораторні ознаки високої ймовірності виникнення загострення патологічного процесу у ГБС. У більшості хворих виявлялася тяжкість у правому підребер’ї, більшість пацієнтів скаржилися також на слабкість, нездужання, зниження емоційного тонусу. В цілому спостерігалися прояви астенічного, астено-невротичного, рідше астено-депресивного регистру. У цих хворих зберігалася гепатомегалія, іноді і спленомегалія, слабо позитивний симптом Кера (36 осіб; 34,6%) та виражені ознаки вегето-судинної дистонії (ВСД). У низки пацієнтів виявлялися незначні зміни з боку функціональних проб печінки, які характеризувалися вірогідним підвищенням вмісту зв’язаної фракції білірубіну (в середньому в 1,5–1,8 разів; Р<0,05) при близькому до норми рівню загального білірубіну. Виявлено помірне збільшення активності амінотрансфераз у сироватці крові обстежених хворих, зокрема АлАТ була підвищена стосовно норми в 1,2–1,6 рази, АсАТ — 1,1–1,4рази. При цьому індекс де Рітіса (співвідношення АсАТ/АлАТ) становив 0,69±0,02 та 0,74±0,02, що практично відповідало межам норми. Тимолова проба також була дещо вище за норму і досягала рівня 6–6,5 од. Рівень «печінкових» фракцій ЛДГ4+5 був підвищений в середньому в 1,3–1,5 рази. В цілому дані свідчили про суттєве підвищення вірогідності у таких хворих загострення запального процесу в ГБС та характеризували стан пацієнтів як нестійка ремісія коморбідної патології у вигляді ХНХ та ХВГС.
У результаті проведення імунологічних досліджень було встановлено, що до початку проведення реабілітаційних заходів у переважної більшості хворих на ХНХ, сполучений з ХВГС з МСА, мали місце чітко виражені зсуви показників гуморальної ланки імунітету (таблиця 1).
Таблиця 1. Рівень ЦІК та їхній молекулярний склад у хворих на ХНХ, сполучений з ХВГС з МСА, до початку медичної реабілітації (M±m)
| Імунологічні показники | Норма | Групи обстежених хворих | Р | |
| основна (n=62) | зіставлення (n=68) | |||
| ЦІК, г/л | 1,88±0,03 | 2,34±0,06** | 2,31±0,07** | >0,1 |
| (>19S), % г/л | 44,5±2,3 | 24,8±1,2** | 25,9±1,3** | >0,1 |
| 0,84±0,04 | 0,58±0,05* | 0,6±0,06* | >0,1 | |
| (11S–19S), % г/л | 30,5±1,2 | 41,1±1,1** | 39,8±1,2** | >0,1 |
| 0,57±0,04 | 0,96±0,07** | 0,92±0,05** | >0,1 | |
| (<11S), % г/л | 25,0±1,6 | 34,1±1,2* | 34,3±1,1* | >0,1 |
| 0,47±0,03 | 0,8±0,06** | 0,79±0,05** | >0,1 | |
Примітки: вірогідність розбіжності з показником норми * — при Р<0,05, ** — при Р<0,01, Р<0,00і; стовпчик Р — вірогідність розбіжності між показниками основної групи та групи зіставлення.
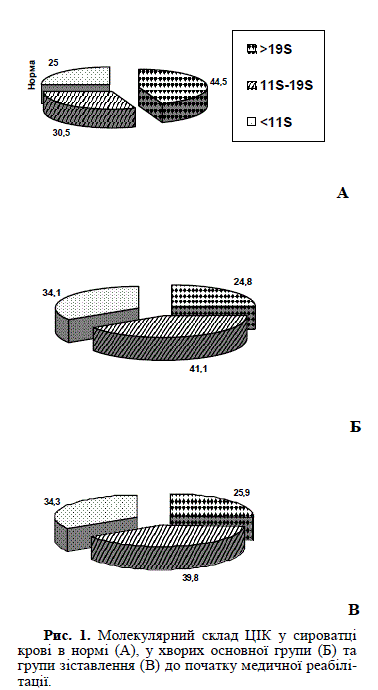
Як видно з таблиці 1, концентрація ЦІК була вище норми в основній групі хворих в середньому в 1,24 рази (при нормі 1,88±0,03 г/л; Р<0,01) та в групі зіставлення — в 1,23 рази (Р<0,01). При цьому підвищення відбувалося переважно за рахунок найбільш патогенних фракцій: середньомолекулярних (11S–19S) та дрібномолекулярних (<11S) (рис.1). Дійсно, абсолютний вміст середньо-молекулярної фракції (11S–19S) в сироватці крові хворих на ХНХ, поєднаний з ХВГС з МСА, був підвищеним в 1,68 рази відносно норми (0,57±0,04 г/л; Р<0,01) в основній групі та в 1,61 рази в групі зіставлення. Стосовно концентрації дрібномолекулярних ІК, то вона була підвищена в середньому в 1,7 рази в основній групі (при нормі 0,47±0,03 г/л; Р<0,01) і в групі зіставлення в 1,68 рази (Р<0,01). В той же час абсолютнаконцентрація великомолекулярних ІК (>19S) у більшості обстежених хворих була нижче норми в середньому в 1,45 рази в основній групі (при нормі 0,84±0,04 г/л; Р<0,05) і групі зіставлення в 1,4 рази (Р<0,05).
Отже, у обстежених хворих на ХНХ, поєднаний з ХВГС з МСА, до початку проведення реабілітаційних заходів відзначено підвищення ЦІК в сироватці крові за рахунок найбільш суттєвого збільшення концентрації середньо- та дрібномолекулярної фракцій ІК, що свідчить про наявність вираженого синдрому імунотоксикозу (Рис.1). При цьому зсуви в обох групах були однотиповими.
При повторному проведені імунологічних досліджень після завершення курсу медичної реабілітації, було встановлено, що у пацієнтів основної групи, які отримували комбінацію антралю та артіхолу, відмічено суттєва позитивна динаміка імунологічних показників (табл. 2).
Виходячи з даних таблиці 2, в основній групі хворих концентрація ЦІК суттєво знизикрові в нормі (А), у хворих основної групи (Б) та лася та досягла верхньої межі норми (Р>0,05).
Таблиця 2. Рівень ЦІК та їхній молекулярний склад у хворих на ХНХ, сполучений з ХВГС з МСА після проведення медичної реабілітації (M±m)
| Імунологічні показники | Норма | Групи обстежених хворих | Р | |
| основна (n=62) | зіставлення (n=68) | |||
| ЦІК, г/л | 1,88±0,03 | 1,9±0,03 | 2,11±0,04* | =0,05 |
| (>19S), % г/л | 44,5±2,3 | 42,6±2,0 | 30,5±1,3* | <0,05 |
| 0,84±0,04 | 0,81±0,04 | 0,64±0,03* | <0,05 | |
| (11S–19S), % г/л | 30,5±1,2 | 31,2±1,0 | 36,4±0,7* | <0,05 |
| 0,57±0,04 | 0,59±0,05 | 0,77±0,04* | <0,05 | |
| (<11S), % г/л | 25,0±1,6 | 26,2±1,2 | 33,1±1,1* | <0,05 |
| 0,47±0,03 | 0,5±0,03 | 0,7±0,04* | <0,05 | |
При цьому також відмічена практично повна нормалізація молекулярного складу ЦІК, що свідчило про ліквідацію синдрому імунотоксикозу у цих пацієнтів. У групі зіставлення також відмічена певна позитивна динаміка з боку вивчених показників, однак менше виражена, ніж у хворих основної групи, тому вони залишилися від’ємними як від норми, так і даних основної групи.
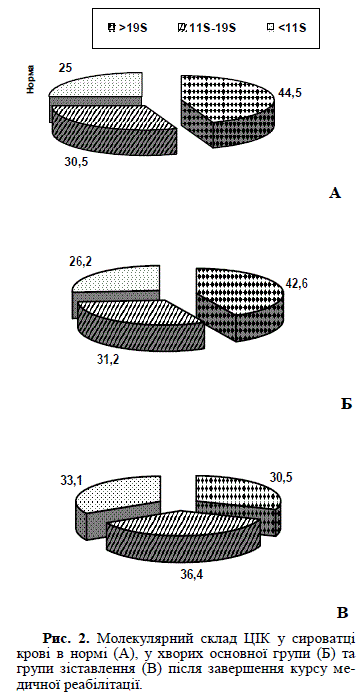
Дійсно, загальний рівень ЦІК у пацієнтів групи зіставлення в цей період обстеження знизився відносно початкового рівня в середньому в 1,1 рази, але зберігався в 1,3 рази вище за норму (Р<0,05) і складав 2,11±0,04 г/л. При цьому зберігався дисбаланс молекулярних фракцій ІК: абсолютний вміст середньомолекулярної фракції ІК (11S–19S) залишився підвищеним в 1,35 рази від норми (Р<0,05) та рівень дрібномолекулярних ІК перевищував показник норми в 1,5 рази (Р<0,05). Концентрація великомолекулярних ІК у більшості пацієнтів групи зіставлення залишалась навпаки нижче норми в середньому в 1,31 рази (Р<0,05).
У результаті клінічних спостережень було встановлено, що істотне поліпшення самопочуття та зникнення астенічних проявів у хворих, які одержували антраль в комбінації з артіхолом, відбувається протягом перших 2–3 тижнів з моменту початку проведення курсу медичної реабілітації. Разом із істотним поліпшенням загального самопочуття хворих і значним зниженням числа скарг, що характеризують психоемоціональний стан, в основній групі також істотно зменшилося число пацієнтів із скаргами, що характеризують ураження гепатобіліарної системи. Так, число хворих із скаргами на наявність тяжкості в правому підребер’ї знизилося в основній групі в 9,4 рази, тоді як в групі зіставлення — в 1,7 рази, склавши після місячного курсу медичної реабілітації відповідно 4,6±2,1% і 24,6±3,9% (Р<0,01). Отже, це свідчить про позитивний ефект комбінації антралю та артіхолу у хворих на ХНХ, поєднаний з ХВГС з МСА. Одночасно відмічається також позитивна динаміка біохімічних показників крові, що характеризують функціональний стан печінки у хворих на ХНХ, сполученого із ХВГС з МСА, основної групи. Так, пов’язана фракція білірубіну зменшилася відносно початкового рівня в 3,2 рази і становила 3,2±0,1 мкмоль/л (Р<0,01). У той же час у групі зіставлення пов’язана фракція білірубіну знизилася до 5,8±0,08 мкмоль/л, що перевищувало норму в 1,2 рази (Р<0,05). Активність АлАТ суттєво зменшилася та досягла меж норми в основній групі, у групі зіставлення також відмічалася позитивна динаміка активності сироваткових амінотрансфераз, однак суттєве менше виражена, ніж в основній групі, тому у цих хворих активність АлАТ та АсАТ на момент завершення реабілітаційних заходів в 1,2 рази вище норми та показника у хворих основної групи (Р<0,05). Тимолова проба у пацієнтів основної групи також знизилася до норми, а в групі зіставлення все ж таки дещо перевищувала межі норми (4,5±0,1 од.; Р<0,05). Отримані дані вказують на високу ефективність застосування в комплексі реабілітаційних заходів комбінації гепатопротектору антралю та препарату з артішоку колючого — артіхолу.
За даними диспансерного нагляду тривалість повноцінної клініко-біохімічної ремісії у хворих з хронічною патологією ГБС (ХНХ, ХВГС) при застосуванні вітчизняного гепатопротектору антралю в комбінації з препаратом рослинного походження артіхолом у 52 (83,9%) пацієнтів основної групи складала 1 рік та більше (період диспансерного нагляду) та у 10 (16,1%) — від 6 до 11 місяців. Отже, клініко-біохімічні показники у цих хворих зберігалися стабільними, працездатність пацієнтів не страждала, вони успішно виконували свою повсякденну роботу, за даними біохімічного обстеження подальшого прогресування патологічного процесу в печінці не відмічено. В групі зіставлення тривалість ремісії в більшості випадків була менше та становила у 41 осіб (60,3%) від 3 до 6 місяців, у 15 пацієнтів (22,6%) — від 7 до 11 місяців, і лише у 12 хворих (17,1%) — 1 рік та більше. Отже клініко-біохімічна ремісія тривалістю 1 рік та більше у хворих основної групи відмічалася в 4,9 рази частіше, ніж у пацієнтів групи зіставлення (Р<0,01).
Висновки
- У більшості хворих на ХНХ, поєднаний з ХВГС з МСА, в періоді диспансерного нагляду виявлялася тяжкість у правому підребер’ї, більшість пацієнтів скаржилися також на слабкість, нездужання, зниження емоційного тонусу. В цілому спостерігалися прояви астенічного, астено-невротичного, рідше астено-депресивного регистру. У цих хворих зберігалася гепатомегалія, іноді і спленомегалія, слабо позитивний симптом Кера (36 осіб; 34,6%) та виражені ознаки вегето-судинної дистонії (ВСД).
- До початку медичної реабілітації у обстежених пацієнтів виявлені дані, що свідчили про суттєве підвищення вірогідності у них загострення запального процесу в ГБС та характеризували стан пацієнтів як нестійка ремісія коморбідної патології у вигляді ХНХ та ХВГС: вірогідне зростання вмісту зв’язаної фракції білірубіну при близькому до норми рівню загального білірубіну; помірне збільшення активності амінотрансфераз у сироватці крові обстежених хворих (АлАТ — в 1,2–1,6 рази, АсАТ — 1,1–1,4 рази), тимолова проба досягала рівня 6–6,5 од та рівень «печінкових» фракцій ЛДГ4+5 був підвищений в 1,3–1,5 рази.
- У пацієнтів з ХНХ, поєднаним з ХВГС з МСА, в періоді медичної реабілітації при імунологічному дослідженні виявлені порушення з боку гуморальної ланки імунітету, які характеризувались підвищенням концентрації ЦІК в 1,23–1,24 рази переважно за рахунок найбільш патогенних середньомолекулярних (11S–19S) та дрібномолекулярних (<11S) фракцій ЦІК.
- Включення до комплексу медичної реабілітації гепатопротектору антралю та засобу рослинного походження з артишоку колючого — артіхолу сприяє нормалізації вмісту ЦІК у крові та їхнього молекулярного складу, тобто ліквідації синдрому імунотоксикозу.
- За даними диспансерного нагляду тривалість повноцінної клініко-біохімічної ремісії у хворих з хронічною патологією ГБС (ХНХ, ХВГС) при застосуванні антралю та артіхолу у 52 (83,9%) пацієнтів основної групи складала 1 рік та більше та у 10 (16,1%) — від 6 до 11 місяців, тобто клініко-біохімічна ремісія тривалістю 1 рік та більше відмічалася у цих хворих в 4,9 рази частіше, ніж у пацієнтів групи зіставлення.
- Таким чином, включення антралю та артіхолу до комплексу реабілітаційних заходів у хворих на ХНХ, поєднаний з ХВГС з МСА, патогенетично доцільно та клінічно перспективно і може бути рекомендовано для широкого застосування в клінічній практиці.
- В подальшому вважаємо доцільним вивчити вплив даної комбінації препаратів на стан редокс-системи глутатіону в періоді диспансерного нагляду хворих зі сполученою хронічною патологією ГБС.
Література
- Антраль: інструкція для медичного застосування препарату / Затверджена 17.08.2007 р. Наказом МОЗ України № 483.
- Артіхол: інструкція для медичного застосування препарату / Затверджена 16.11.2006 р. Наказом МОЗ України № 758.
- Гарник Т.П., Фролов В.М., Пересадін М.О. Артишок полевой (Супага scolymusL.) как пищевое и лекарственное растение, перспективное для создания новых гепатозащитных препаратов // Проблеми екологічної та медичної генетики iклінічної імунології: 3б. наук. праць. — Київ; Луганськ; Харків, 2006. — Вип. 6 (75). — С. 17–36.
- Карпов С.Ю., Крель П.Е. Клиническая характеристикаи особенности течения хронического гепатита С низкой степени активности // Клиническаямедицина. — 2005. — № 1. — С. 14–19.
- Крылов А.А. К проблеме сочетаемости заболеваний // Клиническая медицина. — 2000. — № 1. — С.56–58.
- Лапач С.Н., Чубенко А.В., Бабич П.Н. Основные принципы применения статистических методов в клинических испытаниях. — Киев: Морион, 2002. — 160 с.
- Малый В.П., Звягинцева Т.Д., Титовский С.П. HCV-инфекция (острая и хроническая) клинико-патогенетическая и терапевтические аспекты. — Киев, 2005. — 292 с.
- Москаленко В.Ф., Харченко RB., Голубчиков М.В. Заболевания гепатобилиарной системы (распространенность, нерешенные проблемы) // Зб. наукових праць співр. КМАПО ім. П.Л. Шупика. — 2000. — Вип. 9, Кн. 4. — С. 5–10.
- Соцька Я.А. Вплив вітчизняного препарату артішоку колючого — артіхолу на стан системи антиоксидантного захисту у хворих з хронічним некалькульозним холециститом, поєднаним з хронічним вірусним гепатитом С з мінімальним або низьким ступенем активності в періоді медичної реабілітації // Проблеми екологічної та медичної генетики iклінічної імунології: 3б. наук. праць. — Київ; Луганськ; Xap^, 2006. — Вип. 6 (75). — С.224–239.
- Соцька Я.А., Фролов В.М. Вплив фітопрепарату «Артишоку-екстракту Здоров’я» в комбінацій з гепатопротектором «Антралем» на показники ліпопероксидації у хворих на хронічний некалькульозний холецистит, сполучений з хронічним вірусним гепатитом С з мінімальним ступенем активності // Фітотерапія. — 2008. — №2. — С. 29–36.
- Фролов В.М., Рычнев В.Е., Пересадин Н.А Исследование циркулирующих иммунных комплексов их диагностическое и прогностическое значение // Лабораторное дело. — 1986. — № 3. — С. 159–161.
- Фролов В.М., Пересадин Н.А, Бойченко П.К. Диагностическое и прогностическое значение циркулирующих иммунных комплексов у больных // Врачебное дело. — 1990. — № 6. — С. 116–118.
- Фролов В.М., Романюк Б.П., Петруня А.М. Иммунные и микрогемодинамические нарушения при патологии печени и их коррекция. — Луганск: Изд-во ЛГМУ, 1994. — Т. 1. — 194 с.
- Фролов В.М., Гарник Т.П., Соцька Я.А., Борзенко І.А. Ефективність комбінацій антралю та фітопрепаратів в комплексі медичної реабілітації хворих на хронічний вірусний гепатит С, сполученийіз хронічним некалькульозним холециститом // Укр. медичний альманах. — 2006. — Том 9, № 1. — С. 150–157.
- Фролов В.М., Григорьева А.С. Антраль — эфективный препарат для лечения заболеваний печени // Укр. медичний часопис. — 2003. — № 2 (34). — C. 65–68.
- Rizetto M. Therapy of chronic viral hepatitis: a critical review // Ital. J. Gastroenterol. Hepatol. — 1999. — № 31. — Р. 781–793.
Стаття надана мовою оригіналу






