
 Статья
Статья
 26.02.2025
26.02.2025
Особенности терапии предменструального синдрома у женщин с эндометриозом
Н.Ф. ЗАХАРЕНКО д. мед. н., главный научный сотрудник отделения эндокринной гинекологии Института педиатрии, акушерства и гинекологии НАМН Украины В.П. КОВБАСИЙ к. мед. н., медицинская сеть «Добробут», Киев И.П. МАНОЛЯК Институт педиатрии, акушерства и гинекологии НАМН Украины
Актуальность:
В настоящее время одной из наиболее актуальных проблем в гинекологии является предменструальный синдром (ПМС), поскольку он относится не только к числу широко распространенных, но наименее изученных состояний.
Согласно последним данным, ПМС можно рассматривать как функциональное расстройство центральной нервной системы (ЦНС) вследствие действия неблагоприятных внешних факторов на фоне врожденной или приобретенной лабильности гипоталамо-гипофизарно-овариальной системы [1].
Частота предменструального синдрома колеблется, по данным различных авторов, в пределах 25–90%, причем у каждой женщины симптомы индивидуальны, встречаются в разных сочетаниях, у 10% – ярко выражены, существенно снижают качество жизни и, в ряде случаев, приводят к потере трудоспособности [2]. ПМС представляет собой многогранный симптомокомплекс, включающий более 150 симптомов и проявляющийся нервно-психическими, вегетососудистыми и обменно-эндокринными нарушениями в лютеиновую фазу ментруального цикла.
ПМС является полиэтиологической и полисимптомной патологией, в возникновении которой определенную роль играют личностные, средовые факторы и преморбидный фон. Известно, что ПМС до 29 лет наблюдается у 20% женщин, в возрасте 30-39 лет – у 47% и в период 40-50 лет у 55% женщин. По данным некоторых авторов у практически здоровых женщин ПМС встречается в 28,8% случаев. По данным С.М. Шардина (1991), среди женщин с хроническими заболеваниями желудочно-кишечного тракта ПМС встречается в 92% случаев, с сахарным диабетом — в 72,4% случаев. Часто наблюдается ПМС у женщин с психическими заболеваниями: при маниакально-депрессивном психозе у 86,4% больных, при психопатиях — в 68,3%, при неврозах — в 81,4%, при алкоголизме — в 72,2%, у больных с пороками сердца он встречается в 41,5%. У пациенток с генитальным эндометриозом ПМС имеет место в 95% и его лечение, наряду с купированием симптомов эндометриоза, приобретает особое значение [3].
Существует множество теорий, пытающихся объяснить происхождение данного патологического состояния. Взгляды на причины и механизм его развития менялись с расширением знаний о физиологии и патологии менструального цикла. Среди патогенетических теорий ПМС выделяют гормональную, теорию водной интоксикации, циклического авитаминоза, теорию недостатка магния и кальция в организме, теорию нарушения синтеза простагландинов, аллергическую теорию и др. Однако ни одна из них в полной мере не объясняет возникновения всех симптомов, характерных для предменструального синдрома.
Исторически первой является гормональная теория, предложенная Р. Франком, согласно которой ПМС – следствие относительной или абсолютной гиперэстрогении в лютеиновой фазе цикла, что является абсолютно характерным для женщин с эндометриозом. Повышение уровня эстрогенов в сыворотке крови вызывает задержку натрия, что приводит к накоплению межклеточной жидкости и отекам. Кроме того, дополнительный синергичный эффект достигается путем влияния эстрогенов на секрецию альдостерона путем изменения дофаминэргической передачи или обмена дофамина. Прогестерону присуще натрий-диуретическое действие, что способствует повышению диуреза. При гиполютеинизме, характерном для ПМС, жидкость задерживается в тканях, что клинически проявляется периферическими отеками, масталгией, вздутием живота, увеличением массы тела, артралгиями. Раздражительность, головную боль и некоторые другие неврологические и психические проявления ПМС можно объяснить отечностью головного мозга.
Развитие психопатологической составляющей ПМС в последние годы объясняется также особенностями метаболизма прогестерона в ЦНС. Известно, что эстрогены и прогестерон яичникового происхождения поступают в ткань головного мозга с кровотоком. Кроме того, они продуцируются непосредственно в головном мозге клетками глии и играют важную роль во всех процессах, происходящих в ЦНС. При нормальном метаболизме прогестерона в ЦНС образуется аллопрегненолон, обладающий способностью стимулировать А-рецепторы гамма-аминомасляной кислоты (ГАМК) и повышать активность хлоридных ионных канальцев нейронных мембран, обеспечивая анксиолитический (седативный) эффект. В случае нарушения метаболизма прогестерона, образуется прегненолон и прегненолона сульфат, являющиеся антагонистами как А-, так и В-ГАМК рецепторов. Наличие В-ГАМК рецепторов не только в ЦНС, но и в других системах и органах, может в некоторой степени объяснить полиморфизм клинических проявлений ПМС. Другими гормональными факторами развития ПМС являются: изменение содержания андрогенов (тестостерона, дегидроандростерона этихоланолона), кортикостероидов; гипо- и гипертиреоидные состояния; гиперпродукция гормонов передней (пролактина), задней (вазопрессина и альдостерона) и средней (меланоцитстимулирующего гормона) доли гипофиза.
Гиперчувствительностью к гормонам можно в определенной степени объяснить старую аллергическую теорию ПМС. Доказательством наличия аллергического статуса при ПМС являются положительные внутрикожные пробы с препаратами половых стероидных гормонов, выполняемые во 2-ю фазу цикла. Считается, что одним из сенсибилизирующих факторов служит генитальная инфекция грибковой этиологии, провоцирующая развитие парадоксальных реакций на собственные гормоны.
Одной из распространенных теорий патогенеза ПМС является так называемая теория водной интоксикации. Однако до сегодняшнего времени дискутируется вопрос о задержке и перераспределении воды в организме. Ретенция жидкости объясняется нейро-эндокринными нарушениями с вовлечением системы ренин-ангиотензин-альдостерон.
Доказана роль простагландинов (ПГ) в патогенезе ПМС. Поскольку ПГ являются универсальными тканевыми гормонами, которые синтезируются практически во всех органах и тканях, нарушение их продукции может проявляться разнообразием клинических эффектов: депрессией, раздражительностью, нервозностью, масталгией, болью и вздутием живота, повышением температуры тела и др. Многие из них сходны с состоянием гиперпростагландемии. Рядом авторов, изучавшим содержание простагландинов, отмечено, что дефицит содержания простагландинов Е1 вызывает депрессию, а его избыток может привести к аффективным расстройствам. Увеличение уровня простагландина Е2 приводит к сужению интракраниальных сосудов и развитию мигрени. Во время лютеиновой фазы эндометрий выделяет простагландины, не вызывает сомнения, что нарушение их секреции приводит к дисменорее и ПМС [3]. Изменение гемодинамики малого таза в виде гипертензии и спазма сосудов или длительной вазодилатации и венозного застоя, вызванного недостатком магния и повышением концентрации простагландинов F2a, способствует гипоксии клеток, накоплению аллогенных веществ, раздражению нервных окончаний и возникновению боли внизу живота перед менструацией и в первые ее дни [3].
Отмечено, что у здоровых женщин перед менструацией количество магния в эритроцитах увеличивается. У женщин же страдающих ПМС, наоборот, количество магния снижается на 20-40% по сравнению с нормой. Имеются данные, что у женщин с ПМС концентрация ионизированного магния во 2-ю фазу цикла понижена, а коэффициент Са2+/Mg2+ повышен [5]. Дефицит магния и В6 часто сочетаются друг с другом – дефицит пиридоксина сопровождается клиническими симптомами, которые часто наблюдаются при недостаточности магния [4]. Некоторые авторы указывают на связь возникновения симптомов предменструального синдрома с недостаточностью витамина В6 в лютеиновую фазу (теория циклического авитаминоза) [3]. При дефиците магния и витамина В6 развивается недостаток прогестерона и относительная гиперэстрогения [3]. Выявлено, что в свою очередь избыток эстрогенов может привести к недостатку витамина В6, который является коферментом в заключительной стадии образования дофамина и серотонина [3]. Причиной недостаточности дофамина в мозге может быть и дефицит магния. Поэтому прием магния и витамина В6 помогает изменить ситуацию, приводит к увеличению дофамина и серотонина, что облегчает симптомы ПМС. Магний и витамин В6 способствуют увеличению выработки простагландина E1 и снижению таковой простагландина Е2 из ненасыщенных жирных кислот, поступающих с пищей, тем самым положительно влияя на симптомы депрессии и мигрени при ПМС [3]. Магний приводит к снижению выработки простагландина ПГF2а клетками эндометрия, его релаксации и уменьшению выраженности циклического болевого синдрома [3]. Магний вызывает гипертрофию гломерулярной зоны коры надпочечников, секретирующей альдостерон, что ведет к задержке жидкости. В клинической практике дефицит магния чаще всего становится очевидным не только при ПМС, но и при миоме матки, эндометриозе, патологическом климаксе и дисменорее (состояниях, имеющих особую выраженность у женщин с эндометриозом).
Учитывая высокую частоту развития ПМС на фоне эндометриоза, его полиэтиологичность, противоречивость теорий патогенеза, вариабельность клинической картины, актуальной является оптимизация способов терапии предменструального синдрома с учетом его особенностей при генитальном эндометриозе.
Материалы и методы исследования:
С целью изучения эффективности терапии в исследование нами включено 45 женщин репродуктивного возраста от 19 до 40 лет (средний возраст составил 34,4±6,3 года) с ПМС средней степени тяжести. Группы исследования были рандомизированы по возрасту, формам ПМС и генитального эндометриоза.
І группу исследования составили 15 пациенток, отказавшиеся от терапии Дидрогестероном, получающие Магникум 1 таб. 3 раза в день по схеме, ІІ группу – 15 пациенток, отказавшиеся от терапии Дидрогестероном, получающие Магникум 2 таб. 3 раза в день по схеме и группу сравнения – 15 пациенток, получающих терапию Дидрогестероном, согласно рекомендациям нормативних документов.
Предложен следующий режим лечения Магникумом: с 14 по 28-й день цикла в течение 3-х месяцев.
Схема терапии Дидрогестероном: по 10 мг 2 раза в день с 16-го по 25-й день менструального цикла в течение 3-х месяцев.
Все пациентки перед лечением и обследованием подписали информированное согласие на участие в исследовании.
С целью мониторинга эффективности терапии нами проводилась субъективная и объективная оценка динамики клинических симптомов согласно специально разработанной анкете через 3 и 6 месяцев после лечения. Независимая оценка болевого синдрома проводилась по методу многомерной семантической дескрипции с применением Мак-Гилловского опросника (McGill Pain Questionnaire)
[В. В. Кузьменко и соавт., 1986].
Полученные цифровые данные обрабатывали с применением современных методов медицинской статистики с помощью программы Excel Microsoft Office с применением критерия Стьюдента. Разницу между величинами, которые сравнивали, считали достоверной при p<0,05.
Результаты исследования.
Клиническая картина ПМС у исследуемых женщин характеризовалась следующими симптомами: дисменорея имела место у 31 пациентки (68,9%), раздражительность – у 37 (82,2%), слабость — у 18 (40%), депрессия – у 23 (51,1%), нарушение пищевого поведения – у 14 (31,1 %), мастодиния – у 32 пациенток (71,1%), отечность век, лица, пальцев рук – у 17 (37,8%), увеличение массы тела во 2-й фазе цикла – у 15 (33,3%), головная боль – у 14 (31,1%), акне – у 7 (15,6%), повышение температуры – у 3 пациенток исследуемых групп (6,7 %). Вышеперечисленные симптомы относятся преимущественно к нервно-психической и отечной формам ПМС.
Через 3 месяца терапии Магникумом в І, ІІ-й группах исследования и Дидрогестероном (в группе сравнения) отмечено существенное уменьшение количества женщин с дисменореей по сравнению с показателем до лечения (53,3 и 60 %, соответственно в І, ІІ-й, 46,7 % в группе сравнения, против 82,2% до терапии; p<0,05).
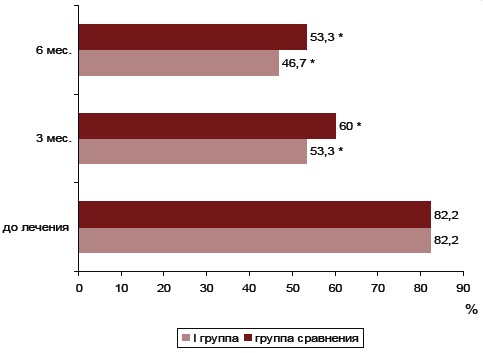
Рис. 1. Динамика удельного веса женщин с дисменореей І группы в ходе терапии.
1. * – разница достоверна относительно показателя количества женщин с дисменореей до лечения, (p<0,05).
При этом значимой разницы между количеством женщин с дисменореей в І, ІІ-й группах исследования по сравнению с показателем в группе сравнения выявлено не было (53,3 и 60 % соответственно в І, ІІ-й группе, против 46,7 % в группе контроля; p>0,05). Через 6 месяцев от начала терапии показатели количества женщин с дисменореей существенно не изменились в группах исследования по сравнению с такими через 3 месяца от начала лечения (60 и 46,7% в І, ІІ-й группе против 53,3 и 60% соответственно; p>0,05). (Рис. 1., Рис. 2.)
.jpg)
Благодаря многомерной семантической дескрипции согласно Мак-Гилловскому опроснику нами обнаружен существенно более высокий средний показатель рангового индекса боли у женщин І, ІІ-й групп исследования и группы сравнения до начала терапии (49,2±2,5; 56,1±2,7 и 51,3±1,5 балла) относительно соответствующих показателей через 3 месяца от начала терапии (5,4±0,6; 4,1±0,8 и 6,2±0,9 балла), (p<0,05). При этом, статистически значимой разницы между средними показателями рангового индекса боли у женщин І, ІІ-й групп исследования относительно группы сравнения не выявлено (49,2±2,5; 56,1±2,7 баллов, соответственно в І, ІІ-й группах в сравнении с 51,3±1,5 балла в группе сравнения; p>0,05). Через 6 месяцев после лечения средние показатели рангового индекса боли существенно не изменились относительно таких через 3 месяца после терапии в группах исследования (5,4±0,6; 4,1±0,8 и 6,2±0,9 балла, соответственно в І, ІІ-й и группе сравнения, против 3,2±0,8; 2,8±0,6 и 5,3±0,5 балла), (p>0,05). (Рис. 3.)
Характер болевых ощущений у женщин групп исследования, который оценивали по среднему значению количества выбранных дескрипторов, существенно ниже через 3 мес. после лечения, что свидетельствует о статистически значимом снижении интенсивности болевого синдрома при ПМС (15,1±0,6, 10,2±0,8 и 14,3±0,5 баллов, соответственно в І, ІІ-й и группе сравнения, против (2,3±0,8, 3,2±0,4 и 2,9±0,8 баллов), (p<0,05). При этом существенной разницы средних показатей количества выбранных дескрипторов через 3 мес. после лечения между группами исследования не виявлено (15,1±0,6, баллов соответственно в І, ІІ-й группах в сравнении с 14,3±0,5 баллами в групе сравнения; p>0,05). Через 6 месяцев после лечения средние показатели количества избранных дескрипторов существенно не изменились относительно таких через 3 месяца после терапии в группах исследования (2,3±0,8, 3,2±0,4 и 2,9±0,8 балла, соответственно в І, ІІ-й и группе сравнения, против 2,8±0,3; 1,7±0,5 и 2,1±0,7 балла), (p>0,05). (Рис. 4).
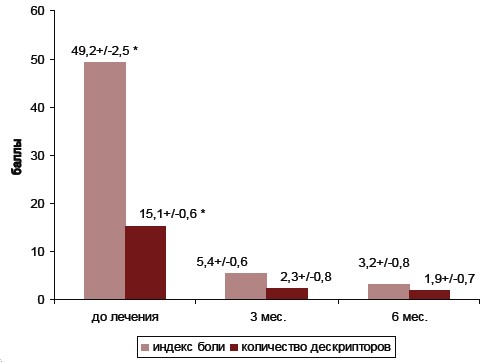
Рис. 3. Средние параметры боли у женщин І группы исследования согласно Мак-Гилловскому опроснику.
1. * – разница достоверна относительно показателя через 3 и 6 мес. после лечения (p<0,05).
.jpg)
Рис. 4. Средние параметры боли у женщин ІІ группы исследования согласно Мак-Гилловскому опроснику.
1. * – разница достоверна относительно показателя через 3 и 6 мес. после лечения (p<0,05).
Таким образом, мониторинг клинических симптомов через 6 месяцев от начала терапии выявил отсутствие статистически значимых изменений количества пациенток с дисменореей в сравнении с соответствующими показателями через 3 месяца как в І и ІІ группе исследования, так и в группе сравнения, что может свидетельствовать в пользу эффективности лечения дисменореи Магникумом по 1 или 2 таб. 3 раза в день с 14 по 28-й день цикла в течении 3-х месяцев сравнимой с терапией Дидрогестероном по 10 мг 2 раз в день с 16 по 25-й день цикла.
Нами выявлена положительная динамика симптомов негативной аффектации (раздражительности и депрессии) у женщин групп исследования. Так, показатель количества женщин с проявлениями раздражительности имел тенденцию к снижению через 3 месяца терапии в сравнении с исходным до лечения во всех группах наблюдения (66,7; 73,3 и 60%, соответственно в І, ІІ-й и группе сравнения, против 82,2 % до начала терапии). Предложенные нами схемы лечения можно считать эффективными и в отношении проявлений депрессии (46,7; 40 и 33,3 %, соответственно в І, ІІ-й и группе сравнения, против 51,1 % до начала терапии). При этом существенной разницы между показателями количества женщин с симптомом раздражительности и депрессии в группах наблюдения относительно соответствующего показателя в группе сравнения через 3 мес. после терапии выявлено не было. Через 6 месяцев от начала лечения показатели количества женщин с симптомами раздражительности и депрессии в группах исследования значимо не изменились относительно таковых через 3 месяца после лечения (66,7; 73,3 и 60% женщин с симптомом раздражительности, соответственно в І, ІІ-й и группе сравнения до терапии, против 53,3; 60 и 46,7 % через 6 месяцев после). Аналогичная ситуація имела место и в отношении женщин с проявлениями депрессии (46,7; 40 и 33,3 %, соответственно в І, ІІ-й и группе сравнения до терапии, против 40; 33,3 и 26,7 % через 6 месяцев после). Полученные нами данные свидетельствуют о достаточной клинической эффективности терапии Магникумом по 1 таб. 3 раза в день с 14-го по 28-й день цикла 3 месяца сравнимой с таковой при лечении Магникумом по 2 табл. 3 раза в день, а также при использовании Дидрогестерона 10,0 мг с 16-го по 25–й день менструального цикла с целью купирования симптомов негативной аффектации.
В ходе исследования выявлена статистически значимая положительная динамика симптомов, вызванных задержкой жидкости у женщин с ПМС: отечности, масталгии, увеличения массы тела. Так, показатель количества женщин с симптомами отечности существенно снизился через 3 месяца терапии в сравнении с исходным в группах наблюдения (20; 13,3 и 26,7 %, соответственно в І, ІІ-й и группе сравнения, против 37,8 % до начала терапии), (p<0,05). Через 6 месяцев выше перечисленные показатели значительно не изменились относительно соответствующих показателей через 3 месяца после терапии как в І, так и во ІІ-й группе исследования (Рис. 5., Рис. 6.).
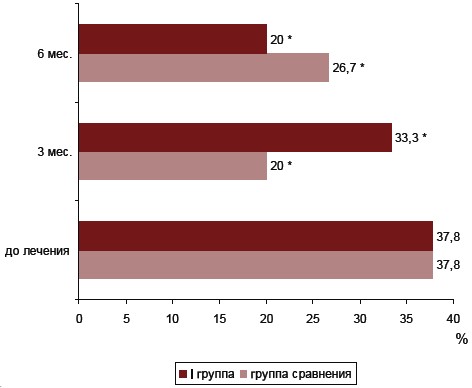
Рис. 5. Динамика показателя отечности у женщин І группы наблюдения в ходе терапии.
1. * – разница достоверна относительно показателя количества женщин с отечностью до лечения, (p<0,05).
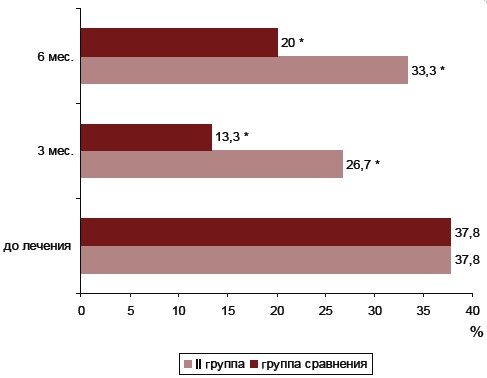
Рис. 6. Динамика показателя отечности у женщин ІІ группы наблюдения в ходе терапии.
1. * – разница достоверна относительно показателя количества женщин с отечностью до лечения, (p<0,05).
Предложенные нами схемы лечения оказались эффективными и в отношении уменьшения масталгии (46,7; 40 и 33,3 %, соответственно в І, ІІ-й и группе сравнения через 3 мес, против 71,1% до начала терапии), (p<0,05). Через 6 месяцев выше перечисленные показатели значительно не изменились относительно соответствующих через 3 месяца после терапии в ІІ-ой группе исследования, в І-й же группе наблюдалось достоверное снижение количества женщин с масталгией ( 60 % через 3 мес. терапии против 33,3 % через 6 месяцев; p<0,05). (Рис. 7., Рис. 8.).
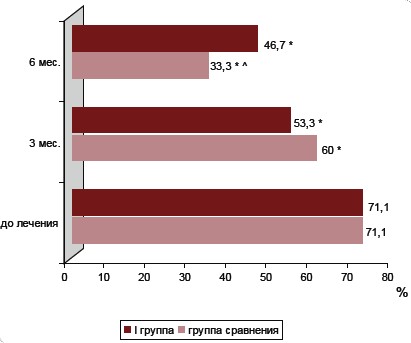
Рис. 7. Динамика показателя масталгии у женщин І группы наблюдения в ходе терапии.
- * – разница достоверна относительно показателя количества женщин с масталгией до лечения, (p<0,05),
- ^ – разница достоверна относительно показателя количества женщин с масталгией через 3 месяца после лечения, (p<0,05).
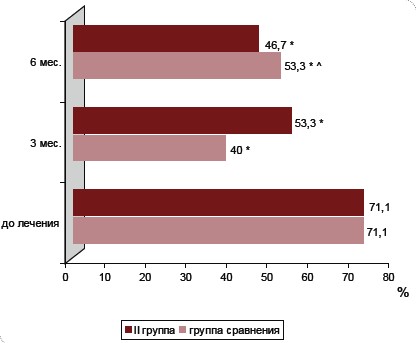
Рис. 8. Динамика показателя масталгии у женщин ІІ группы наблюдения в ходе терапии.
- * – разница достоверна относительно показателя количества женщин с масталгией до лечения, (p<0,05).
Существенная позитивная динамика наблюдалась нами и в отношении снижения массы тела у женщин групп исследования через 3 мес. после терапии (20, 13,3 и 6,7%, соответственно в І, ІІ-й и группе сравнения, против 33,3% до лечения), (p<0,05). При этом статистически значимой разницы между выше описанными показателями в группах наблюдения относительно группы сравнения через 3 мес. после терапии выявлено не было. Через 6 месяцев от начала терапии показатели количества женщин с симптомом увеличения массы тела в группах исследования существенно не изменились в сравнении с такими через 3 месяца от начала терапии (Рис. 9., Рис. 10.).
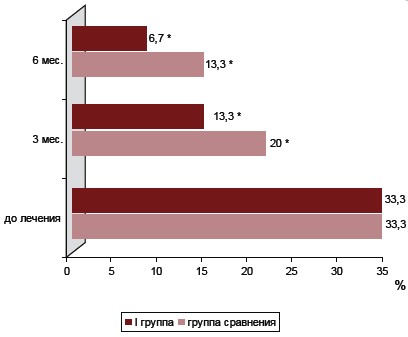
Рис. 9. Динамика показателя снижения массы тела у женщин І группы наблюдения в ходе терапии.
1. * – разница достоверна относительно показателя количества женщин до лечения, (p<0,05).
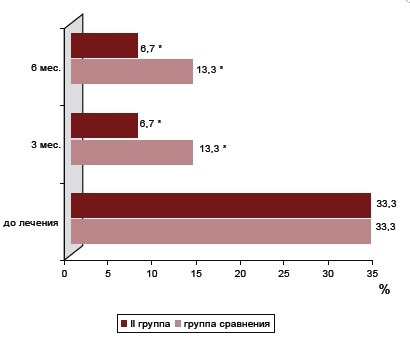
Рис. 10. Динамика показателя снижения массы тела у женщин ІІ группы наблюдения в ходе терапии.
1. * – разница достоверна относительно показателя количества женщин до лечения, (p<0,05).
Полученные нами данные свидетельствуют в пользу клинической эффективности схем лечения Магникумом сравнимой с таковой при лечении Дидрогестероном в отношении симптомов вызванных задержкой жидкости у женщин с ПМС .
Головная боль наблюдалась у 31,1 % женщин до лечения, пожалуй является единственным симптомом цефалгической формы ПМС, выявленным нами в процессе исследования. Головная боль дергающего характера наиболее часто локализовалась в височной области и не сопровождалась повышением артериального давления. В ходе лечения мы наблюдали позитивную тенденцию развития симптома головной боли через 3 месяца терапии у женщин всех групп исследования (20; 33,3 и 26,7 %, соответственно в І, ІІ-й и группе сравнения, против 31,1% до лечения), (p>0,05). Следует отметить, что существенной разницы между количеством женщин с симптомом головной боли в І, ІІ-й группах исследования относительно группы сравнения выявлено не было через 3 месяца после лечения. При этом через 6 месяцев от начала лечения рецидивов головной боли не наблюдалось (26,7 и 20 %, соответственно в І, ІІ-й группе через 6 месяце терапии против 20 и 33,3 % через 3 месяца), что свидетельствует в пользу эффективности схем лечения Магникумом сравнимой с терапией Дидрогестероном.
В то же время, нами не отмечено существенно положительной динамики в отношении проявлений симптомов слабости, нарушения пищевого поведения, повышения температуры до субфебрильной, акне через 3 и 6 месяцев после терапии во всех группах исследования.
Выводы:
- Клиническая картина ПМС на фоне генитального эндометриоза характеризуется доминированием симптомов отечной, нервно-психической и цефалгической форм ПМС.
- Предложенные нами схемы лечения Магникумом по 1 или 2 таб. 3 раза в день с 14 по 28-й день цикла в течении 3-х месяцев сравнимы по эффективности с терапией Дидрогестероном особенно в отношении отечной формы и некоторых симптомов нервно-психической и цефалгической форм ПМС.
- Вышеуказанное позволяет нам рекомендовать схему терапии Магникумом по 1 таб. 3 раза в день с 14 по 28-й день цикла в течении 3-х месяцев как терапевтически эффективную и экономически целесообразную.
Литература
- Татарчук Т. Ф., Венцковская И. Б., Шевчук Т. В. Предменструальный синдром – междисциплинарная проблема // Мистецтво лікування. – 2004. –№ 4 (010). – С. 36 – 43.
- Пересада О. А. Предменструальный синдром: патогенез, клинические проявления, лечение // Медицинские новости. – 2010. – №8. – С. 15–18.
- Прилепская В. Н., Межевитинова Е. А., Сасунова Р. А., Иванова Е. В. Роль магния в патогенезе предменструального синдрома // Российский вестник акушера-гинеколога. – 2012. – № 3.
- Майоров М .В., Жученко С. И. Применение препаратов магния в амбулаторной гинекологии //Медицинские аспекты здоровья женщины. – 2011. – № 1. – С. 14 –18.
- Gonda X., Telek T., Juhasz G., Lazary J., Vargha A., Bagdy G. Patterns of mood changes throughout the reproductive cycle in healthy women without premenstrual dysphoric disorders. Prog Neuropsychopharmacol Biol Psychiatry 2008; 32: 8: 1782-1788.





