
 Статья
Статья
 05.02.2025
05.02.2025
Ефективність та безпека застосування ірбесартану при лікуванні хворих та інвалідів внаслідок артеріальної гіпертензії з дуже високим додатковим ризиком
Лисунець О.М., Ханюкова І.Я. Український державний НДІ медико-соціальних проблем інвалідності
Актуальність проблеми лікування та розробка схем медичної реабілітації пацієнтів та інвалідів внаслідок артеріальної гіпертензії (АГ) з високим ризиком подальших серцево-судинних ускладнень при наявності супутньої ішемічної хвороби серця (ІХС), цукрового діабету (ЦД) обумовлена широкою розповсюдженістю цих захворювань в популяції, частим їх сполученням, несприятливим взаємним впливом, а також значимістю їх медико-соціальних наслідків за показниками первинної та накопиченої інвалідності в Україні [1, 2].
Дослідження останніх десятиріч довели провідну роль активації ренін-ангіотензинової системи (РАС) в розвитку АГ і судинних ускладнень. Виявлення локальних тканинних РАС в клітинах нирок, серця, мозку, ендотелії судин і інших тканинах з’явилося зворотнім моментом в переосмисленні значущості цієї системи в розвитку патології різних органів. Препаратами, які пригнічують активність локально-тканинних РАС є інгібітори ангіотензинперетворюючого ферменту (ІАПФ) і блокатори ангіотензинових рецепторів (БРА). Всі міжнародні дослідження, в яких ставилася задача порівняти ефективність цих препаратів з іншими класами антигіпертензивних засобів (блокаторами кальцієвих каналів, бета-блокаторами, діуретиками), показали, що при рівному антигіпертензивному ефекті ІАПФ і БРА володіють значущо більш вираженою кардіо- і нефропротективною дією. Найбільш переконлива ефективність цих препаратів при наявності ЦД та діабетичної нефропатії [7]. У хворих на АГ та ЦД органопротективна спрямованість препаратів обумовлена не лише їх антигіпертензивною активністю, а також здатністю локально в тканинахблокувати дію ангіотензина II (АТ II), зменшуючи його патологічний вплив на функцію нирки, нормалізуючи тканинну гемодинаміку і архітектоніку. Поряд з цим, препарати класу БРА мають переваги в порівнянні з ІАПФ. Найважливішими з них є більш повна блокада дії АТ II; одночасна стимуляція АТ2-рецепторів на фоні блокади АТІ-рецепторів, що призводить до додаткового судинорозширюючого ефекту; відсутність стимуляції брадикініна, що дозволяє уникнути таких побічних реакцій, властивих ІАПФ, як кашель, кропив’янка, алергічні набряки. В останніх європейських Рекомендаціях по лікуванню АГ (2007) суттєво розширились показання до використання цього класу препаратів як засобів першого ряду або у складі комбінованої терапії в лікуванні АГ.
В клінічній практиці в даний час використовуються різні блокатори АТІ-ангіотензинових рецепторів, які володіють вираженою і тривалою антигіпертензивною дією. Представляє інтерес аналіз ефективності застосування ірбесартана. Отримані результати ряду клінічних випробувань продемонстрували його високу переносимість і ефективність як органопротектора у хворих на АГ з ураженням органів-мішеней, здатність ірбесартана забезпечувати ренопротекцію у хворих на АГ з діабетичною нефропатією на різних стадіях захворювання [8, 9, 11, 13 ]. Метою даного дослідження було вивчення антигіпертензивної ефективності та безпечності застосування ірбесартана (Ірбетана) в лікуванні хворих на АГ з високим ризиком серцево-судинних ускладнень; вивчення впливу терапії, що проводилась, на клінічні маркери ураження нирок та функціональний стан ендотелію судин.
Матеріал і методи
В дослідження включено 32 хворих (з них 19 чоловіків і 13 жінок у віці 58,5±4,5 роки), що були визнані інвалідами внаслідок АГ. Середня тривалість існування АГ склала 12,7±2,1 роки. Критеріями виключення хворих з дослідження були інфаркт міокарду та інсульт протягом 6 місяців до дослідження, важкі захворювання печінки, важка серцева недостатність, наявність термінальних стадій мікросудинних ускладнень ЦД, «офісний» САТ вищий 180 мм рт.ст. або ДАТ вищий 110 мм рт.ст. Серед супутніх станів найчастіше зустрічались стенокардія напруги II-IIIФК, післяінфарктний кардіосклероз — у 24 (75%), ЦД 2 типу у 19 (59,4%) хворих. 6 (18,8%) хворих перенесли лакунарні інфаркти мозку, 5 (15,6%) хворих страждали на персистуючу форму фібриляції передсердь. У 23 (71,9%) хворих виявлялась маркери ураження нирок.
Пацієнти проходили стаціонарне лікування, а потім амбулаторне спостереження в кардіологічному відділенні інституту. Дизайн дослідження передбачав призначення ірбетана з титрацією дози на протязі 2-4 тижнів до цільової — 300 мг/ добу. На початку лікування 16 хворих на ІХС отримували кардіоселективні бета-блокатори в низьких або середніх дозах. Всі хворі приймали статини, аспірин. Тривалість терапії ірбетаном склала 12 тижнів. Пацієнтам проводили обстеження на початку дослідження, а також через 12 тижнів лікування. При контрольних візитах кожні 2 тижні вимірювали рівень АТ, частоту серцевих скорочень, при необхідності — рівень глікемії натщесерце, загальний аналіз сечі; оцінювали будь-які небажані явища і зміни в супутній медикаментозній терапії. Корекцію антигіпертензивної терапії проводили при незадовільному стані хворого.
Цільовим рівнем вважали рівень АТ < 130/80 мм рт.ст. Якщо при прийомі 300 мг ірбесартана протягом 4 тижнів цільові цифри АТ не досягались, хворим в терапію додавали тіазідний діуретик (гідрохлортіазід 12,5–25 мг на добу) або дигідропірідіновий антагоніст кальцію (амлодіпін 5 мг на добу).
Для корекції гіперглікемії пацієнти приймали пероральні сахарознижуючі препарати з групи сульфаніламідів або комбінації сульфаніламідів і бігуанідів, дози яких під час дослідження не корегувалися.
Переносимість препарату вважали доброю за відсутності побічних ефектів, задовільної — при виникненні скороминущих побічних ефектів, щоне вимагали відміни препарату, і незадовільною — при появі побічних ефектів, що потребували відміни препарату.
Всім хворим виміряли «офісний» АТ вранці (8.00-10.00) згідно з рекомендаціями Американської асоціації кардіологів [5]. САТ і ДАТ реєстрували на одній руці в положенні сидячи двічі з інтервалом в 2 хв. Якщо величина АТ відрізнялася більш, ніж на 5 мм рт.ст., проводилося третє вимірювання і обчислювалося середнє значення двох або трьох послідовних вимірювань. Частоту скорочень серця (ЧСС) визначали після другого вимірювання.
Добове моніторування АТ (ДМАТ) проводили за допомогою комплексу «Кардіотехніка 4000АД» (ІНКАРТ, Санкт-Петербург) по стандартній методиці протягом 24-26 годин [14 ]. Аналізували середні денні (д) і нічні (н) значення систолічного та діастолічного АТ, їх варіабельність (стандартне відхилення від середньої величини), добовий індекс АТ (відношення різниці між середнім денним і нічним АТ до середнього денного АТ у відсотках), індекс часу денної і нічної систолічної і діастолічної гіпертензії (відсоток вимірювань АТ, що перевищували 140/90 мм рт. ст.в денний період і 120/80 мм рт. ст. в період сну.
Загальноклінічні і біохімічні дослідження проводились за стандартними методикам в науково-дослідній лабораторії інституту. Визначали загальний аналіз крові, сечі, добові втрати білка з сечею, рівень глюкози, креатинину, сечової кислоти, загального холестерину, тригліцерідів, калію, натрію.
Дослідження рівня екскреції альбуміну проводилось методом гетерогенного твердофазного одностадійного конкурентного аналізу за допомогою набору реактивів «Микроальбумин ЛРАП»/ «Ольвекс диагностикум» (Росія) з використанням біохімічного аналізатора Backman (USA). Швидкість клубочкової фільтрації (ШКФ) розраховувалась за формулою D. Cockcroft та M. Gault (1976).
Для оцінки вазорегулюючої функції ендотелію використовували пробу з потокозалежною ділятацією плечової артерії (ПА) за методикою, розробленою D.S. Celermajerі колегами (1992). Реєструвалися і оцінювалися в динаміці діаметр ПА, лінійна швидкість кровотоку у спокої, діаметр ПА та лінійна швидкість кровотоку після проведення оклюзійної проби. Ендотелій-залежну вазоділятацію артерії (ЕЗВД) розраховували як відносну зміну діаметру артерії протягом проби з реактивною гіперемією, виражену у відсотках. Нормальною вважали реакцію плечової артерії, при якій збільшення її діаметру дорівнювало 10 і більше відсотків від початкового рівня [4, 10]. Дослідження виконувалося на апараті Logic 5 Pro (GE, USA), датчиком з частотою 5 Мгц.
Статистичну обробку результатів проводили в системі Windows Exsel 2003 за допомогою пакету програм, інтегрованих в цю систему. Достовірність різниці середніх показників визначали за допомогою t-критерія Ст’юдента.
Результати обстеження
На момент включення в дослідження 9 (28,1%) хворих мали АГ 1 ступеня, 23 (71,9%) — АГ 2 ступеня. Динаміка офісного САТ, ДАТ і ЧСС на початку лікування і через 12 тижнів представлена в таблиці 1. Спостерігалося прогресивне достовірне зниження показників: середній офісний САТ знизився на 18,5% з 158,7±2,6 до 129,3±3,2 мм рт.ст. (Р<0,05), ДАТ на 12,1% — з 96,3±4,2 до 84,6±3,8 мм рт.ст. (Р<0,05). Зміни в ЧСС не були достовірні: з 72,4±1,5 до 74,3±1,7 уд.в хв (Р>0,05). При використанні монотерапії ірбетаном цільові рівні АТ були досягнуті в 14 випадках (43,8%), в інших було потрібно додавання до лікування додаткових антигіпертензивних засобів: в 15 (46,9%) —гідрохлортиазиду, в 3 (9,4%) — гідрохлортиазиду та амлодипіну.
.jpg)
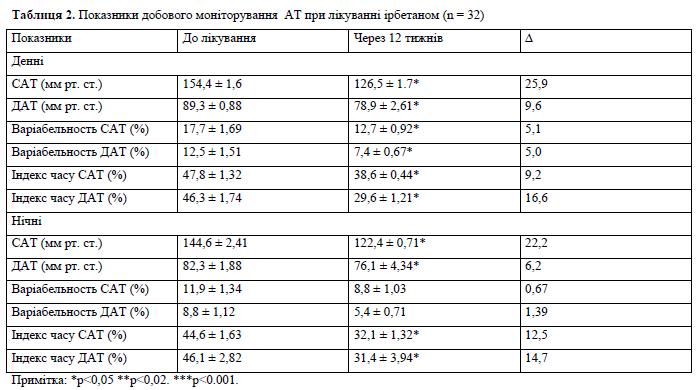
За даними добового моніторування АТ достовірно знизилися показники середнього САТ та ДАТ як в денний, так і в нічний час (табл. 2). Терапія ірбесартаном призводила до зменшення показників «навантаження тиском» в денні та нічні години: достовірно знизився індекс часу САТ, індекс часу і індекс площі ДАТ (р < 0,05). Терапія ірбетаном достовірно знижувала початкову підвищену варіабельність САТ і ДАТ протягом доби.
При дослідженні ЕЗВД при пробі з реактивною гіперемією у 90,6% пацієнтів, включених в дослідження, виявлена недостатня, а у 18,7% навіть парадоксальна реакція ендотелію — вазоконстрикція в ході проведення проби. Середнє значення ЕЗВД плечової артерії склало 4,82±0,49%, що практично в 2 рази менше, ніж у осіб того ж віку без чинників ризику серцево-судинних захворювань. Результати дослідження вазорегулюючої функції ендотелію представлені в таблиці 3.
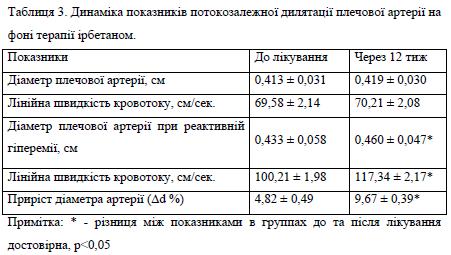
Достовірних відмінностей середнього діаметра плечової артерії до і після курсу лікування відзначено не було (до лікування — 0,413±0,031 і після лікування — 0,419±0,030 р>0,05). Початкова швидкість кровотоку по плечовій артерії дорівнювала 69,58±2,14 м/с.
Через 12 тиж проводима терапія ірбетаном призводило до достовірно значущого приросту діаметра плечової артерії у відповідь на пробу з реактивною гіперемією (з 4,82±0,49% до 9,87±0,39%; р<0,001), що свідчить на користь поліпшення функціонального стану ендотелію. Нормалізацію ЕЗВД, за данними проби з реактивною гіперемією, спостерігали у 28,1% пацієнтів, у 71,9% відмічено поліпшення ЕЗВД. Випадків вазоконстрикції плечової артерії в ході проведення проби з реактивною гіперемією після лікування хворих ірбесартаном виявлено не було.
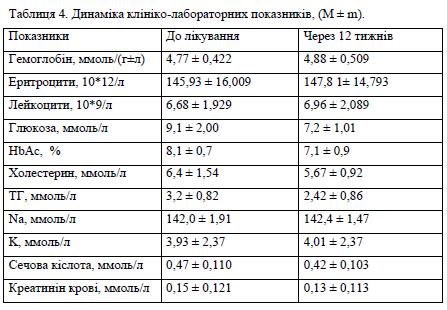
В таблиці 4 представлена динаміка середніх величин вивчених клініко-лабораторних показників у обстежених хворих в процесі лікування. Прийом ірбетана протягом 12 тижнів не викликав достовірних змін в показниках загального аналізу крові. Було відмічено тенденцію до зниження рівнів глюкози, глікозилірованного гемоглобіну, загального холестерину, тригліцерідів. Вірогідних змін рівнів натрію та калію у сироватці крові в ході лікування відзначено не було (р > 0,05). Спостерігалася тенденція до зниження рівнів сечової кислоти (з 0,47±0,110 до 0,42±0,103), креатиніну (з 0,15±0,12 до 0,13±0,11 ммоль/л), що не досягли статистично значущих величин (р > 0,05).
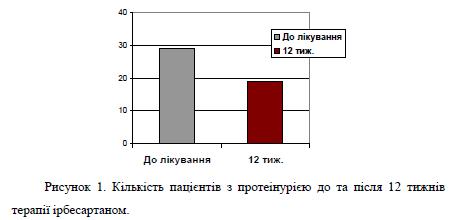
На фоні лікування ірбетаном відмічалось істотне покращення функції нирок. Після 12-ти тижнів терапії мало місце статистично значуще зменшення значень добової протеїнурії (з 0,91±0,67 до 0,52±0,16 г/добу, р < 0,05). У 59,4% хворих, що мали до початку лікування клінічні маркери ураження нирок, наприкінці 12 тижнів лікування протеїнурії виявлено не було. Відмічено також, що антигіпертензивний і антипротеінурічний ефект лікування, що проводився, не відрізнявся у хворих з різними початковими рівнями протеінурії і креатинина сироватки крові, рівнями АТ.
За оцінками пацієнтів, ефект лікування як «дуже добрий» та «добрий» відмічали 27 (84,4%) хворих, поліпшення стану («задовільний» ефект) — 5 (15,6%) хворих. Відсутність ефекту або погіршення стану відмічено не було.
Переносимість препарату вважали дуже доброю. Тільки у одного пацієнта було зафіксовано минущу слабкість на фоні прийому ірбесартану, що не потребувала відміни препарату. На нашу думку це було пов’язано з дуже потужним антигіпертензивним ефектом ірбесартана у цього пацієнта. Побічних реакцій, таких як сухий кашель, ангіоневротичний набряк, алергічні реакції протягом дослідження зафіксовано не було.
Обговорення результатів
В проведеному досліджені продемонстровано, що тривале застосування антигіпертензивного режиму у хворих на АГ з супутніми станами та високим ризиком серцево-судинних ускладнень, що базується на використанні ірбетана у дозі 300мг/доб, має достатньо високий рівень успіху в досягненні цільових значень АТ, зменшенні «навантаження тиском» як в денні, так і в нічні години. Це дуже важливо для хворих на АГ в сполученні з ІХС та/чи ЦД. Масштабні міжнародні дослідження останніх років — ALLHAT, INVESTта ін. свідчать, що ефективна антигіпертензивна терапія значно знижує
частоту розвитку ускладнень ІХС та покращує прогноз у хворого на АГ. В дослідженні UKPDSбуло доведено, що успіх лікування АГ у хворих на ЦД більшою мірою залежить не від якості контролю глікемії, а саме контролю АТ. Разом з тим, як це підкреслюється і іншими дослідниками, у частини пацієнтів з АГ для реального контролю АТ була потрібна багатокомпонентна комбінована терапія.
На фоні проведеної антигіпертензивної терапії ірбетаном отримані позитивні результати покращання вазорегулюючої функції ендотелію. До сьогодні доказано, що ендотеліальна дисфункція є не тільки незмінним атрибутом АГ, а також безпосередньо приймає участь в підтримці та прогресуванні хвороби. Проведене дослідження вазорегулюючої функції ендотелію плечової артерії дозволило оцінити вазо- і органопротекторні можливості фармакотерапії ірбетаном з позицій модуляції продукції NO(10). Корекцію ендотеліальної дисфункції на тлі терапії ірбетаном разом з контролем традиційних чинників ризику атеросклерозу слід розглядати як стратегічну лінію ефективного попередження серцево-судинних ускладнень.
Ризик розвитку серцево-судинних ускладнень та прогресування ураження нирок пропорційно зростає зі збільшенням рівня екскреції білка. Суттєво погіршує реабілітаційний потенціал і прогноз цієї категорії хворих виникнення навіть незначних ознак порушення функції нирок. Тому, особливої уваги заслуговує отриманий антипротеїнуричний ефект після проведеного лікування ірбетаном. Оцінка добової екскреції білка з сечею може бути як кількісною ознакою ураження нирок, так і використовуватися в динаміці для оцінки ефективності терапевтичних заходів (Сіренко Ю.М., 2008 р.). Зменшення середніх значень рівня протеїнурії з 0,91±0,67 до 0,52±0,16 г/добу та зникнення у 59,4% хворих клінічних маркерів ураження нирок визначає у ірбетана його істотний ренопротективний потенціал, що відмічався і іншими авторами [8, 12].
Важливо підкреслити добру переносимість ірбетана в ході тривалого спостереження. В жодному випадку не виникла необхідність його відміни.
Про добру переносимість ірбесартана в різних групах хворих, у тому числі у осіб з ХПН, повідомляють також інші автори [8, 11, 12]. Безпека проведення антигіпертензивного лікування, що базується на використанні ірбесартана, підтверджується також відсутністю у наших пацієнтів негавних змін рівнів глюкози, загального холестерину, тригліцерідів, натрію і калія сироватки крові в процесі лікування, сечової кислоти.
Висновки
- Терапія ірбетаном в добовій дозі 300 мг на протязі 12 тиж надавала багатоплановий коригуючий вплив на показники добового профілю АТ, призводила до достовірного зниження АТ протягом доби; нормалізацію індекса навантаження тиском в денний і нічний час, достовірно знижувала початкову підвищену варіабельність САТ і ДАТ протягом доби. Лікування ірбетаном виявилося ефективним у 43,8% хворих при монотерапії і дозволило досягти цільових значень АТ у всіх пацієнтів при комбінованій терапії.
- Застосована терапія достовірно покращувала показники функції ендотелію. Стан ендотелій-залежної вазоділатації через 12 тиж достовірно зріс з 4,82±0,49% до 9,67±0,39% (р<0,001). ЕЗВД нормалізувалася, за даними проби з реактивною гіперемією, у 28,1% пацієнтів, у 71,9% — відмічено її суттєве поліпшення.
- Ірбетан є ефективним і безпечним антигіпертензивним препаратом, який має виражену антипротеінурічну дію. Після 12-ти тижнів терапії мало місце статистично значуще зменшення значень добової протеїнурії з 0,91±0,67 до 0,52±0,16 г/добу (р < 0,05). У 59,4% хворих, що мали до початку лікування клінічні маркери ураження нирок, наприкінці 12 тижнів лікування протеїнурії виявлено не було. Антигіпертензивний і антипротенурічний ефект лікування не відрізнявся у хворих з різними початковими рівнями протеінурії.
- На тлі терапії препаратом відмічено позитивний вплив на показники, що характеризують вуглеводний обмін (зниження рівня глікемії натщесерце і зниження рівня глікозилированного гемоглобіну).
- Добра переносимість препарату, поступовий гіпотензивний ефект і зручність однократного прийому забезпечили високу прихильність пацієнтів до лікування.
- Ірбесартан може використовуватись в індивідуальних програмах медичної реабілітації інвалідів внаслідок АГ з високим ризиком подальших серцево-судинних ускладнень.
Література
- Артериальная гипертензия у особых категорий больных / Под редакцией В.Н.Коваленко, Е.П.Свищенко. — К. Морион. — 2009. — 374 с.
- Основні показники інвалідності та діяльності медико-соціальних експертних комісій України за 2008 рік. // Аналітико-інформаційний довідник. В.В. Маруніч, А.В. Іпатов, Ю.І. Коробкін та інш. — Пороги, 2009.
- Сиренко Ю.М. Гіпертонічна хвороба й нирки: як лікувати більш ефективно. // Артеріальна гіпертензія. — 2008. — №1. — С.81–88.
- Britten M., Schuchinger V. The role of endothelial function for ischemic manifestations of coronary atherosclerosis // Herz 1998; 23 (2): P. 97–105.
- ChobanianA.V., BakrisG.L., Black H.R.,Cushman W.C., Green L.A., Izzo J.L., et al. Seventh report Joint National Committee on Prevention, Detection, Evaluation, and Treatment High Blood Pressure: JNC 7 Report // JAMA. 2003;289:P.2560–2572.
- Dostal D.E. The cardiac rennin-angiotensin system: novel signaling mechanisms related to cardiac growth and function// Regul Pept 2000; 91:1–11.
- Epstein M, Sowers J.R. Diabetes mellitus and hypertension// Hypertension 1992; 19: P.403–418.
- Lewis EJ et al. Renoprotective effects of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes// N Engl J Med 2001; 20 (345) 12: 851–860.
- Lijen P, Petrov V. Renin-angiotensin system, hypertrophy and gene expression in cardiac myocites// J Mol Cell Cardiol 1999; 31: P.949–970.
- Lierberman E, Knab S, Creager M. Nitric oxide mediates the vasodilator responses to flow in humans // Circulation 1994; 90: P.138.
- Malmqist K et al. Regression of ventricular hypertrophy in human hypertention with irbesartan //J Hypertens 2001; 19 (6): P.1167–1176.
- Parving H.H., Lehnert H., Brochner-Mortensen J. et al. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes// N Engl J Med 2001; 345 (12): P.870–878.
- Verdecchia P, Schillaci G, Borgioni C et al. Prognostic significance of serial changes in left ventricular mass in essential hypertension// Circulation 1998; 97: P.48–54.
- White W. Blood Pressure Monitoring in Cardiovascular Medicine and Therapeutitics // New Jersey: Humana Press. 2001. — 308 p.
Стаття надана мовою оригіналу






