
 Article
Article
 04.03.2025
04.03.2025
Профілактика тромботичних ускладнень в гінекології з допомогою комплексного використання прямих антикоагулянтів й препаратів венотонічної та ангіопротекторної дії
Л.Б.Маркін, К.Л.Шатилович, Л.П.Кропивницька, І.Г.Киричинська Львівський національний медичний університет імені Данила Галицького, м.Львів; Львівська обласна клінічна лікарня, м.Львів
Prevention of thrombotic complications in gynecology by the complex usage of direct anticoagulants and drugs with venotonic and angioprotective actions
L.B.Markin, K.L.Shatylovych, L.P.Kropyvnytska, I.H.Kyrychynska
The results of complex prevention of thrombotic complications in the postoperative period in patients with varix desease, who were operated about the uterine fibroid with the usage of direct anticoagulants and systemic venotonic drug Normoven have been analized. The possibility of the usage of Normoven in the prevention of phlebothrombosis in women with varicose veins of the lower extremities was proved.
Keywords: varicose desease, thrombotic complications, uterine fibroid, Normoven.
В останні роки відзначається неухильне зростання частоти тромботичного ураження вен, що пов’язано із загальним постарінням населення, збільшенням поширеності онкологічних захворювань, все більш частим виникненням спадкових і набутих порушень системи гемостазу, неконтрольованим прийомом гормональних засобів [4]. Тромботичні ускладнення, особливо тромбоз глибоких вен (ТГВ) і тромбоемболія легеневої артерії (ТЕЛА), займають 3 місце серед причин смерті, а від ТЕЛА, за статистикою, гине 0,1% населення земної кулі щорічно. Більше 25% випадків ТГВ і ТЕЛА відбувається безпосередньо при різних оперативних втручаннях, в тому числі і гінекологічного профілю [2,5,8].
Незважаючи на профілактичні заходи, які проводяться з урахуванням груп ризику розвитку тромботичних ускладнень в ранньому післяопераційному періоді, частота венозних тромбоемболічних ускладнень залишається досить високою. У зв’язку з цим логічним є припущення про те, що існують додаткові, невраховані критерії, які відіграють істотну роль у визначенні ступеня ризику розвитку тромбозу в системі нижньої порожнистої вени.
Факторами, ініціюючими виникнення ТГВ, є, насамперед, оперативне втручання (хірургічна агресія активує систему згортання крові), наркоз (міорелаксанти викликають дилатацію внутрішньом’язевих вен і уповільнення відтоку крові з нижніх кінцівок), тривалість оперативного втручання більше 1 год. Цікавим є факт, що в половині випадків ТГВ починає формуватися вже на операційному столі [6, 7].
Отже, проблема ефективності проведення тромбопрофілактики залишається актуальною по сьогоднішній день. Завданням профілактики ТГВ і ТЕЛА є попередження або хоча б зменшення ризику розвитку ТГВ і його наслідків шляхом впливу на різні патогенетичні механізми тромбоутворення.
Мета дослідження
Удосконалити лікувально-профілактичні заходи з метою попередження розвитку тромботичних ускладнень у хворих на міому матки після оперативного втручання шляхом комплексного використання антикоагулянтів прямої дії та препарату венотонічної й ангіопротекторної дії НОРМОВЕНУ.
Матеріали та методи
Під спостереженням знаходилось 50 пацієнток з варикозною хворобою (ВХ) вен нижніх кінцівок, оперованих з приводу фіброміоми матки в об’ємі надпіхвової ампутації матки без додатків (18%) або з додатками (26%) та екстирпації матки без додатків (12%) або з додатками (44%), яким проводилась профілактика ТГВ та ТЕЛА у до- та післяопераційному періодах. У всіх пацієнток важкість захворювання відповідала клінічному класу С1-С3 за міжнародною класифікацією (СЕАР) [1] і включала наступні ознаки:
- телеангіектазії або ретикулярні варикозні вени;
- «гудучі» болі в гомілках і стопах, більш виражені після тривалої ходьби, стоянні або наприкінці дня;
- пастозність, перехідний набряк нижньої третини гомілок і стоп;
- судомні посмикування м’язів ніг.
У 4 випадках мала місце набрякова форма посттромбофлебітичного синдрому.
Пацієнтки були розподілені на наступні групи:
І група спостереження – 10 пацієнток з хронічною венозною недостатністю (ХВН) 0-І стадії, віднесених до групи низького ризику виникнення післяопераційних тромботичних ускладнень (за класифікацією Ch. Samama, 1999), які отримували неспецифічну профілактику (рання активізація після втручання, механічна компресія (лікувальний компресійний трикотаж І-ІІ класу компресії);
ІІ група спостереження – 20 пацієнток з ХВН ІІ-ІІІ стадії, віднесених до групи середнього або високого ризику розвитку тромботичних післяопераційних ускладнень, які крім неспецифічних методів профілактики отримували низькомолекулярний гепарин (клексан). Залежно від маси тіла призначались наступні дози клексану: менше 50 кг – 0,2 мл; 50-70 кг – 0,4 мл, більше 70 кг – 0,6 мл підшкірно. Перша ін’єкція проводилась за 12 годин до операції, друга ін’єкція – через 12 годин після операції, потім I раз на добу протягом 10 днів [3].
ІІІ групу спостереження склали 20 пацієнток середнього або високого ступеню ризику, які додатково отримували препарат НОРМОВЕН у дозі 500 мг двічі на день щонайменше за 5 діб до оперативного втручання та протягом 30 діб після останнього.
Як відомо, Нормовен надає флебопротекторного (шляхом підвищення тонусу венозної стінки і зменшення венозного застою), протинабрякового (шляхом зниження проникності капілярів, збільшення їх резистентності, покращення мікроциркуляції та лімфатичного дренажу) і протизапального ефекту (шляхом),; а також пригнічення активності лейкоцитів і синтезу медіаторів запалення.
Всім хворим до і після операції проводилися нижчеперелічені обстеження:
- загальноклінічні;
- ультразвукове дослідження органів малого тазу (апарат фірми ALOKA IPC-1550);
- допплерометрія вен малого тазу та нижніх кінцівок (апарат фірми Sono Scape 1000).
Дослідження системи гемостазу проводилось до операції, на 2 та 5 добу після операції на базі лабораторії «СИНЕВО» і включало визначення наступних показників: концентрації фібриногену в плазмі крові, активованого часткового тромбопластинового часу (АЧТЧ), активованого часу рекальцифікації (АЧР), протромбінового індексу (ПТІ), протромбінового часу (ПТЧ), тромбінового часу (ТЧ), а також Д-димеру, активності протеїну С, співвідношення МНО/INR (при прийомі антикоагулянтів).
Ефективність запропонованої терапії проводилась клінічно на основі скарг пацієнток. Оцінювались наступні симптоми: біль і відчуття важкості у нижніх кінцівках наприкінці дня, зниження толерантності до статичних навантажень, наявність судом у литкових м’язах. Всі прояви захворювання оцінювали у балах за візуальною аналоговою шкалою: 0 – відсутність симптому, 2 – рідке явище, 4 – часта поява, що не впливає на загальний стан, 6 – виразний ступінь, який погіршує загальний стан, впливає на активність та сон.
Статистична обробка результатів проводилась з використанням програм Microsoft Excel 7.0 та Statistica 6.0.
Результати дослідження та їх обговорення
Середній вік хворих в I групі склав 46,2 ± 2,4, в II групі – 47,5 ± 2,8, а в III – 47,3 ± 3,3 роки. Як видно, пацієнтки всіх груп дослідження за віковими показниками були порівнювані між собою. Середня тривалість операцій хворих груп спостереження при надпіхвовій ампутації матки склала 76±10 хв (min. 50 хв; max. 100 хв), при розширеному втручанні – 85±112 хв (min. 75 хв; max. 130 хв). Тривалість стаціонарного лікування у хворих І групи, в середньому, склала 8,4 ± 4,3 дні (від 6 до 21 дня), у ІІ групі – 8,2 ± 4,8 днів (від 6 до 30 днів), а у ІІІ групі – 6,5 ± 3,8 днів (від 6 до 8 днів).
Основними скаргами, пов’язаними з міомою матки, були: наявність менометрорагій, що призводять до анемії, синдром здавлення сусідніх органів (порушення функції сечового міхура і прямої кишки, важкість внизу живота). Нами було відмічено, що менометрорагії, які призводять до анемії, у хворих ІІ і III групи зустрічались майже в 2 рази частіше, ніж у пацієнток I групи (рис. 1).
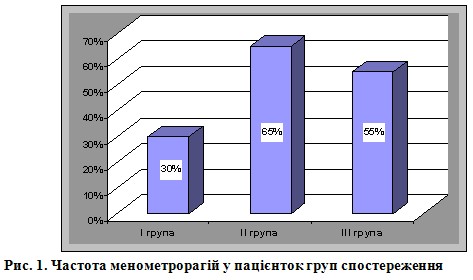
У хворих I групи середній розмір матки разом з міоматозними вузлами склав 12-13 тижнів (min.8-9 тижнів; max. 15-16 тижнів). З них у 2 (20%) мав місце швидкий ріст міоматозних вузлів. У хворих II та ІІІ груп середній розмір матки разом з міоматозними вузлами склав 17-18 тижнів (min. 11-12 тижнів; max. 24-25 тижнів). Швидкій ріст міоматозних вузлів у даних групах мав місце у 10 (50%) та 9 (45%) випадках, відповідно (рис. 2).
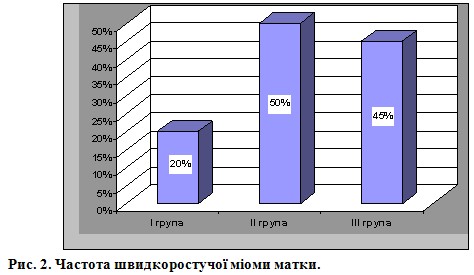
При вивченні структури і частоти екстрагенітальної патології виявлено, що у всіх хворих з посттромбофлебітичним синдромом (n=4) зустрічалось ожиріння, у однієї пацієнтки мало місце гостре порушення мозкового кровообігу в анамнезі. За частотою іншої екстрагенітальної патології всі 3 групи хворих були порівнювані між собою.
Аналіз результатів дослідження соціально-біологічного та акушерсько-гінекологічного анамнезу пацієнток дозволив виділити додаткові чинники розвитку ВХ та ХВН, а саме – великий розмір пухлини матки, швидкий ріст міоматозних вузлів, наявність менометрорагій, що призводять до анемізації хворих.
Дослідженню системи гемостазу у обстежених хворих приділялась особлива увага. Слід відзначити більш виражені гіперкоагуляційні порушення у хворих ІІ та ІІІ груп порівняно з пацієнтками І групи спостереження (табл. 1).
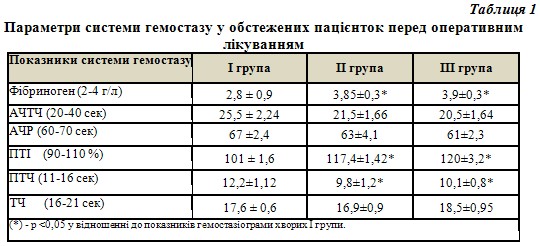
У пацієнток, які перенесли гістеректомію і тривалість втручання у яких перевищувала 90 хв, на 2 день післяопераційного періоду зміни гемостазіологічних показників носили більш грубий характер, порівняно з хворими, які перенесли надпіхвову ампутацію матки. Відбувалося статистично достовірне збільшення рівня фібриногену, ПТІ, зниження АЧТЧ, ТЧ, зростання рівня D-димеру та зниження рівня протеїну С (табл. 2).
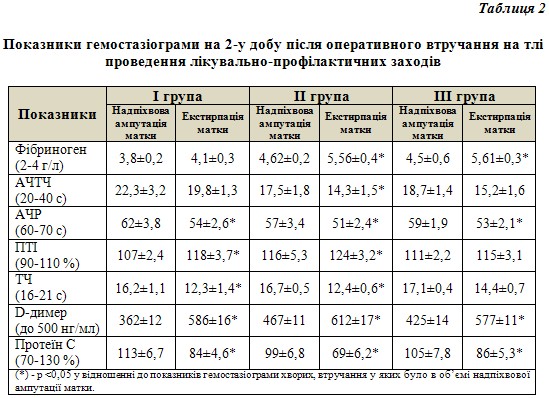
Слід відмітити, що у трьох пацієнток власне після гістеректомії (1-ї – з першої і 2-х – з ІІ групи спостереження) на 4-6 добу післяопераційного періоду був виявлений тромбоз підколінної та/або великої підшкірної вени, що вимагало хірургічного лікування (в одному випадку), початку або пролонгування терапії прямими антикоагулянтами протягом 3 місяців з переходом у непрямі антикоагулянти. Отже, частота венозних тромбозів у хворих, прооперованих в об’ємі екстирпації матки, становила 10,7%. Серед пацієнток після надпіхвової матки тромботичних ускладнень у післяопераційному періоді не було.
Враховуючи вище викладене, пацієнтки, які перенесли гістеректомію, як основного методу лікування міоми матки, за об’ємом та тривалістю оперативного втручання можуть бути віднесені до високого ступеню ризику розвитку тромботичних ускладнень у ранньому післяопераційному періоді.
В результаті проведених комплексних лікувально-профілактичних заходів на 5 добу післяопераційного періоду відмічена виразна позитивна динаміка показників гемостазу у більшості пацієнток всіх груп спостереження (табл.3).
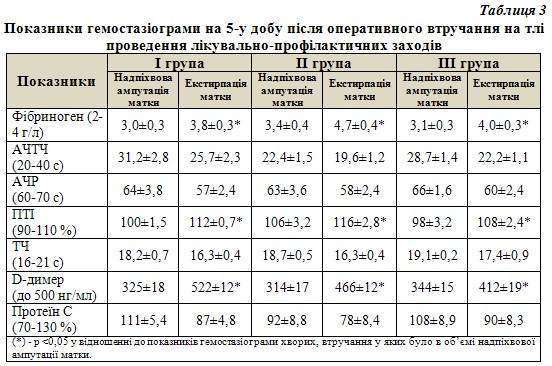
Необхідно підкреслити відсутність тромботичних ускладнень у пацієнток ІІІ групи спостереження, що пов’язано не тільки із застосуванням антикоагулянтної профілактики, але і терапії, спрямованої на покращення мікроциркуляції, лімфодренажу та ліквідацію явищ тканинної гіпоксії на фоні комбінованого прийому діосміну та гесперидину.
При оцінці клінічної картини перебігу ВХ відчутне зменшення виразності симптомів відмітили 12 пацієнток з ІІІ і жодна пацієнтка з І та ІІ груп спостереження. Так, 9 жінок (45%) відмітили відсутність вечірнього болю у ногах, болю після ходьби або тривалого перебування у вертикальному положенні. Зменшення больового синдрому до «незначного дискомфорту» мало місце у 5 (25%) пацієнток. З 19 пацієнток, яких непокоїли набряки гомілок і стоп, у 6 вони майже зникли і не були відмічені при обстеженні. На фоні комплексної терапії не спостерігалось прогресування варикозного процесу.
Таким чином, використання різних методів неспецифічної та специфічної профілактики післяопераційних тромботичних ускладнень дозволило уникнути розвитку тромбозу вен нижніх кінцівок у 100% пацієнток ІІІ групи, зменшити виразність симптомів ВХ та покращити якість життя у 60% випадків.
Висновки
1. Найбільш значущими додатковими критеріями, що підвищують ступінь ризику виникнення ВХ та розвитку тромботичних ускладнень в ранньому післяопераційному періоді у хворих на міому матки, є: великий розмір пухлини матки, швидкий ріст міоматозних вузлів, наявність менометрорагій, що призводять до анемізації хворих, об’єм та тривалість оперативного втручання.
2. Профілактика тромботичних ускладнень із застосуванням комплексу прямих антикоагулянтів та венотоніку НОРМОВЕН є ефективним засобом, що призводить до нормалізації показників гемостазу і знижує ризик розвитку тромботичних ускладнень у післяопераційному періоді до мінімуму.
Список літератури
- Золотухин И.А. Классификация хронических заболеваний вен CEAP: инструкция по применению // Приложение к журналу Consilium Medicum. Хирургия. – 2009. – № 1. – С. 64–68.
- Наказ Міністерства охорони здоров’я від 15.01.2014 №34. «Уніфікований протокол екстреної медичної допомоги: Тромбоемболія легеневої артерії».
- Никульников П.И., Влайков Г.Г., Гуч А.А. Лечение хронической венозной недостаточности нижних конечностей. Новые альтернативы // Кровообіг та гемостаз. – 2008. – №1. – С.76-78.
- Савельев В.С. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений / В.С. Савельев, Е.И. Чазов, Е.И. Гусев, А.И. Кириенко и др. // Флебология. – 2010. – № 1(2). – С. 5-6.
- Сенчук А.Я., Венцковский Б.М. Тромбоэмболические осложнения в акушерстве и гинекологии. – К.: МАККОМ. – 2003. – 360 с.
- Тарабрин О.А., Туренко А.В., Щербаков С.С. Использование бемипарина в комплексной профилактике и коррекции нарушений гемокоагуляции у больных раком тела матки на этапах хирургического лечения // Здоровье женщины. – 2010. – № 4 (50). – С. 130-133.
- Тер-Ованесов М.Д., Маджуга А.В. Тромботические осложнения в онкологии: опыт, реализованный на практике // Практическая онкология. – 2001. – №1(15). – С.25-32.
- Cohen A.T. Assessment of venous thromboembolism risk and the benefit of thromboprophylaxis in medical patients // Thromb. Haemost. – 2005. – № 94. – Р. 750-759.
- Samama Ch.M., Samama M.M. Prevention of venous thromboembolism // Congress of European Society of Anaesthesiology. – Amsterdam, 1999. – Р. 39-43.
Стаття надана мовою оригіналу





