
 Article
Article
 04.03.2025
04.03.2025
Ефективність лікування хворих на остеоартроз у поєднанні з цукровим діабетом 2-го типу з підвищеною масою тіла залежно від ступеня ожиріння
Л.В. Журавльова, М.О. Олійник Харківський національний медичний університет
Резюме. Мета дослідження. Вивчення впливу діацереїну на перебіг остеоартрозу (ОА) та динаміку показників запального процесу (цитокінів та С-реактивного протеїну) у хворих з поєднаним перебігом ОА, цукрового діабету (ЦД) 2-го типу та ожирінням. Матеріали та методи. Було обстежено 35 хворих (10 чоловіків та 25 жінок), середній вік 57,511,13 років, з поєднаним перебігом ОА та ЦД 2 типу. Результати та обговорення. На фоні проведеної терапії у хворих з поєднаним перебігом ОА, ЦД 2-го типу та ожирінням відзначено зменшення болі, скутості, покращення функції суглобів, а також визначено зниження рівня прозапальних цитокінів та рівня СРП. Висновки. Отримані дані показали позитивний вплив препарату діацереїн на артрологічний статус хворих на остеоартроз у поєднанні з ЦД 2-го типу та ожирінням.
Ключові слова: остеоартроз, цукровий діабет 2-го типу, ожиріння, діацереїн, цитокіни.
Одним з найпоширеніших ревматичних захворювань є остеоартроз (ОА)[1]. За впливом на стан здоров’я серед усіх захворювань ОА займає 4-е місце у жінок та 8-е у чоловіків. ОА часто виникає на фоні ожиріння. Крім того, часте поєднання ожиріння з цукровим діабетом (ЦД) 2-го типу та метаболічним синдромом [2,3]. Перш за все, це стосується ОА колінних суглобів, при якому виявлено виражену залежність між ІМТ і ризиком захворювання [4]. З віком втрати працездатності у хворих на гонартроз порівнянний з ризиком хворих на серцево-судинні захворювання, і вище, ніж при іншій патології.
Порушення регуляції синтезу й секреції сигнальних речовин жировою тканиною може бути сполучною ланкою, за допомогою якої ожиріння і інсулінорезистентність (ІР) стають факторами ризику розвитку ОА, оскільки активізують дегенеративно-запальні процеси в суглобових структурах. Адипоцити вісцерального жиру мають високу щільність і чутливість до β-блокаторів (особливо β-3 типу), рецепторів кортизолу й андрогенів, але при цьому – низьку щільність і чутливість інсулінових рецепторів та α-адренорецепторів. ІР являє собою зниження біологічних ефектів інсуліну в різних органах і тканинах. При цьому виникає необхідність у збільшенні кількості інсуліну для компенсації стану ІР. Розвивається компенсаторна гіперінсулінемія, яка посилює поглинання глюкози периферійними тканинами, а також зменшує продукцію глюкози печінкою. Гіперінсулінемія, з одного боку, необхідна для подолання ІР, а з іншого – являє собою патологічний процес, що сприяє виникненню і розвитку метаболічних, гемодинамічних і системних порушень. Порушення метаболізму інсуліну при ожирінні також сприяє погіршенню анаболічних процесів у хондроцитах, якщо враховувати їх чутливість до інсуліну [3,5].
На даний час ожиріння розглядається як стан хронічного підгострого системного запалення, що пов’язано зі збільшенням синтезу прозапальних цитокінів як адипоцитами, так і макрофагами жирової тканини ( інтерлейкину(ІЛ)-1β, фактору некрозу пухлин(ФНП)-α, СРП). При цьому кількість макрофагів, які мігрують в жирову тканину (особливо у вісцеральну), тим більша, чим вища вираженість ІР [6]. Це робить вагомий внесок у розвиток остеоартрозу, який також розцінюється як низькозапальний стан. Запалення посилює руйнування хряща, оскільки прозапальні цитокіни сприяють вивільненню хондроцитами ферментів – матриксних металопротеаз, активаторів плазміногену, що ушкоджують колаген і протеоглікани хряща [7]. Стимулюючи проліферацію фібробластів, синтез простагландинів, фактора активації тромбоцитів, супероксидних радикалів і пригнічуючи синтез колагену та протеогліканів, ФНП-α посилює деструктивні ефекти в суглобових структурах. Істотний вплив на прогресування деградації хряща при остеоартрозі чинить порушення синтезу або дії анаболічних медіаторів – ІФР-1 і ТФР-β, активність яких пов’язана з репарацією хрящової тканини [8]. ІЛ-1 впливє на плазміноген, що сприяє перетворенню його в активний плазмін, який у свою чергу переводить неактивні про-металопротеази в активну форму, посилюючи деградацію позаклітинного матриксу. Катаболічна дія ІЛ-1 проявляється в його здатності стимулювати вироблення хондроцитами і синовіоцитами оксиду азоту, який ушкоджує позаклітинний матрикс. Крім того, оксид азоту, знижуючи концентрацію антагоніста рецептора ІЛ-1, сам активує ІЛ-1 і впливає на апоптоз хондроцитів. ІЛ-1β підвищує екскрецію кальцію, активує остеобласти, що призводить до зниження інтенсивності формування кісткової тканини [9,10,11].
Лікування ОА спрямовано на поліпшення функціональної здатності суглобів, зменшення болю, обмеження прогресування захворювання і поліпшення якості життя хворих. Препаратом, який безпосередньо впливає на вироблення і активність ІЛ-1, є діацереїн. Основна патогенетична дія діацереїну і його активного метаболіту реїну при ОА полягає в пригніченні синтезу ІЛ-1, зниженні експресії рецепторів до ІЛ-1 на поверхні хондроцитів, що сприяє зниженню чутливості клітин до дії цього цитокіну [12,13].
Можна виділити наступні механізми дії діацереїну – екстрацелюлярну дію: зменшення кількості рецепторів до ІЛ-1 на поверхні клітини, за допомогою інгібіювання активності ІЛ-1 на рецепторах ІЛ-1 та інтрацелюлярну дію: попередження активації неактивного ІЛ-1β через ІЛ-1-конвертуючий фермент, попередження AP-1-індуковану MMП-продукцію через його вплив на NFkβ [14].
Проведені дослідження у хворих на ОА показали клінічну ефективність діацереїну, а також наявність у нього ефекту «післядії» [15,16,17]. Також його ефективність при ОА чітко продемонстрована в метааналізі Cochrane, проведеному T.S.Fidelix і співавт. [18]. Однак, досліджень щодо ефективності діацереїну у хворих з коморбідною патологією, а саме, з поєднаним перебігом ОА, ЦД 2-го типу та ожирінням досі не проводилось.
Мета дослідження – вивчення впливу діацереїну на динаміку показників запального процесу (рівень цитокінів та С-реактивного протеїну) та перебіг захворювання у хворих з поєднаним перебігом остеоартрозу (ОА), цукрового діабету (ЦД) 2-го типу з підвищеною масою тіла залежно від ступеня ожиріння.
Матеріали та методи дослідження.
В умовах ревматологічного та ендокринологічного відділень КЗОЗ «Обласна клінічна лікарня – центр екстреної медичної допомоги та медицини катастроф» м. Харкова було відібрано 35 хворих (10 – чоловіків та 25 – жінок) з поєднаним перебігом ОА колінних суглобів та ЦД 2-го типу. Середній вік хворих склав 57,511,13 років. Середня тривалість захворювання на ОА склала -8,29±0,57 років , ЦД 2-го типу – 8,45±0,80 років (таблиця 1).
Діагностику ЦД 2-го типу проводили згідно з критеріями Міжнародної Федерації Діабету (IDF, 2005). Верифікація діагнозу «цукровий діабет 2 типу» проводилась на основі Уніфікованого клінічного протоколу спеціалізованої медичної допомоги: ЦД 2 типу (2012). Проводили вимірювання концентрації глюкози в сироватці крові натще (ГКН), рівня глікозильваного гемоглобіну (НbA1c) та рівень імунореактивного інсуліну (ІРІ). Оцінка рівня ІР проводилась за допомогою НОМА (homeostasis model assessment) — моделі оцінки гомеостазу з розрахуванням індексу ІР (НОМА-IR) за формулою:
HOMA-IR=інсулін (мкОД/мл)×глюкоза (ммоль/л)/22,5.
Критерієм включення до дослідження був субкомпенсований цукровий діабет ( рівень HbA1с не більш 8,5%).
Діагноз ОА колінних суглобів встановлювали на основі діагностичних критеріїв ACR (1991) та Європейської асоціації ревматологів (European League Against Rheumatism, EULAR) 2010 року перегляду. Проводилось клінічне та інструментальне обстеження пацієнтів. Рентгенологічне обстеження виконувалось за допомогою рентгенологічного обладнання КРД-50 Індіаком-02 та РУМ-20-2П2. Стадії ОА оцінювали відповідно з класифікацією J.H.Kellgren та J.S.Lawrens. До дослідження були включені пацієнти з ОА колінних суглобів з I-III рентгенологічною стадією ОА. Інтенсивність болю в суглобах у спокої та при рухах оцінювалась за візуально аналоговою шкалою (ВАШ) та склала ˃40 мм у всіх хворих. Прояви реактивного синовіїту були відсутні.
У пацієнтів абдомінальне ожиріння визначалося відповідно до критеріїв IDF 2005 року – об’єм талії (ОТ) > 94 см у чоловіків та > 80 см у жінок. Використовували індекс співвідношення окружності талії до окружності стегон (ОТ/ОС).
Таблиця 1. Клінічна характеристика хворих
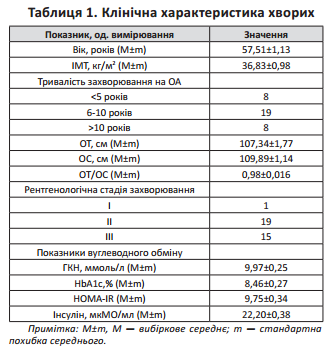
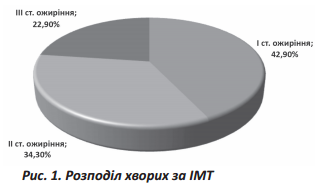
Для всіх хворих обстеження включало вимірювання антропометричних показників: зріст, маса тіла, окружність талії та стегон; обчислення індексу маси тіла (ІМТ=вага×(кг)/рост (м2). Оцінку трофологічного стану проводили згідно з рекомендаціями ВООЗ 1997 року за ІМТ [29]. При обстеженні ожиріння I ступеню було діагностовано у 15 хворих (42,9 %), II ступеню – у 12 хворих (34,3 %), III ступеню ожиріння у 8 хворих (22,9 %), рис. 1.
До початку дослідження хворі не отримували терапії діацереїном. На момент дослідження 21 хворий із 35 для зменшення виразності больового синдрому приймали нестероїдні протизапальні препарати, але прийом їх був ситуаційним або курсовим на протязі 5-7 днів. З метою вивчення впливу діацереїну на перебіг ОА хворим було назначено прийом цього препарату в дозі 50 мг двічі на день під час прийому їжі протягом 3-х місяців. Однак, враховуючи, що в перші два тижні препарат посилює транзиторні функції кішківника на цей період його було призначено у дозі 50 мг на ніч. За наявністю виразного больового синдрому хворі приймали інші протизапальні препарати, але переважно коротким курсом.
Як критерії ефективності використовувались такі показники: вираженість больового синдрому у стані спокою та під час рухів за ВАШ, індекс WOMAC (Western Ontario and McMaster University) з підрахунком балів больового синдрому, скутості, недостатності функції суглобів та загальним балом), тестом Лекена, дані лабораторного дослідження (вміст цитокінів та СРП, показники вуглеводного обміну).
Визначались наступні лабораторні показники:
– рівень С-реактивного протеїну (СРП) в сироватці крові латексним методом.
– рівень IL-1β та ФНП-α визначався імуноферментним методом за допомогою наборів реактивів «Protein Contour» (Росія).
Статистична обробка результатів досліджень включала обчислення середнього арифметичного обчислення середньої похибки середнього арифметичного. При парному порівнянні кількісних показників (до та після лікування) був використаний критерій Вілкоксона. Всі обчислення проводились за довірчої ймовірності 95%, тобто за отримання обчислених значень р < 0,05, результати вважалися статистично значущими. Більшість обчислень проводилася з використанням програмного пакету StatSoft Statisticа версія 10.0.
Результати та їх обговорення
У результаті проведеного лікування із застосуванням діацереїну відмічено покращення загального стану пацієнтів, зменшення виразності больового синдрому, а також помірне покращення функціонального стану суглобів (Табл. 2). Ефект спостерігався через 4-5 тижнів і наростав протягом всього періоду лікування. На тлі безперервного прийому препарату була відмічена позитивна динаміка усіх клінічних показників. Однак слід зазначити, що за наявності ожиріння ІІІ ступеня не було значного покращення рівня болю за шкалою WOMAC, хоча було відмічено покращення функціонального стану й зменшення скутості суглобів.
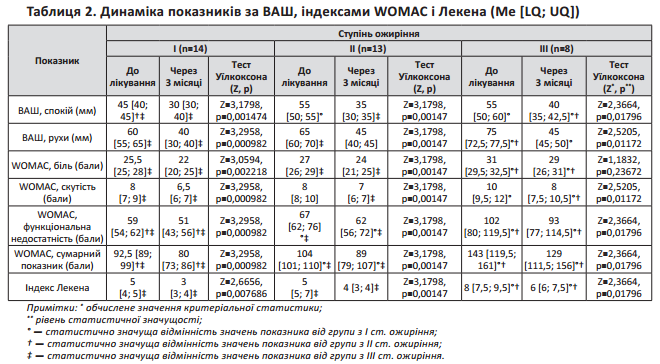
ВАШ було відмічено покращення стану всіх пацієнтів, проте ефективність проведеної терапії для хворих з І та ІІ ступенями ожиріння була більш виразною.
На фоні призначеної терапії було відмічено зниження всіх показників рівня активності цитокінів у пацієнтів із І-им та ІІ-им ступенями ожиріння. У пацієнтів із 3-ім ступенем ожиріння зменшення через 3 місяці рівнів СРП і ФНП- можна вважати статистично значущим, тим часом як IЛ-1 при 3-му ступені ожиріння значно не змінюється (табл. 3).
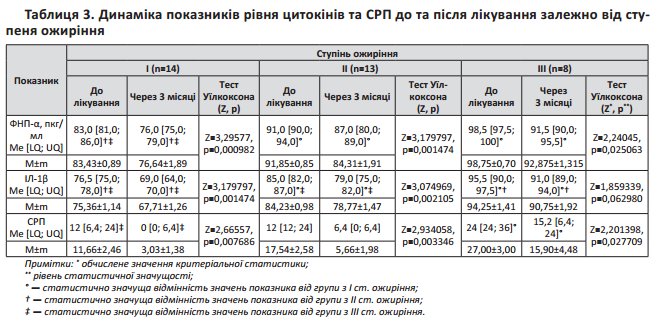
Проведений кореляційний аналіз свідчив на наявність високо статистично значущих залежностей активності цитокінів від ступеня ожиріння, які зберігалися як до лікування, так і після нього. Причому, якщо для СРП ця залежність була помірної сили (=0,48; p=0,000044), то рівні ФНП- і IL1- були пов’язані зі ступенем ожиріння дуже сильними позитивними кореляціями (=0,81 та =0,79; p=0,00000 відповідно ).
Щодо перебігу ЦД 2 типу на фоні зазначеної терапії погіршення стану хворих визначено не було (Рис.2.).
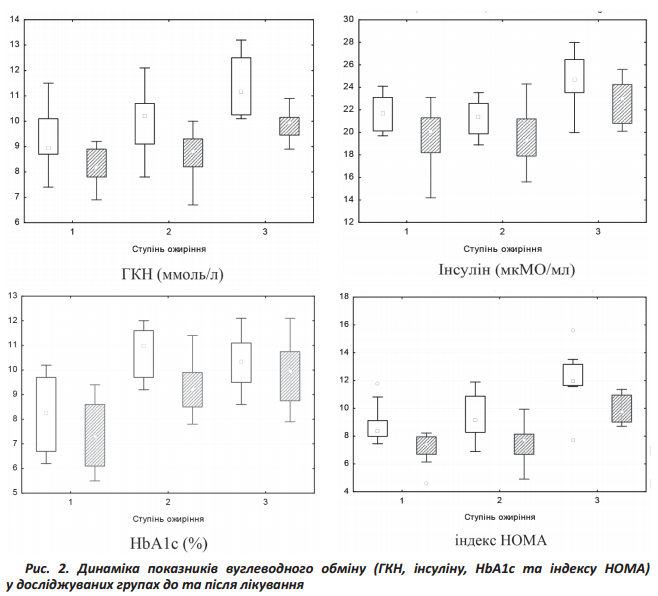
Треба зазначити, що переносимість діацереїну була задовільною. Побічні ефекти відмічались лише у 2-х пацієнтів у вигляді діареї, що призвело до відміни препарату у одного з них. Після відміни діацереїну, побічні ефекти невелювались самостійно. Алергічних реакцій не спостерігалось.
Висновки.
- Прийом діацереїну призводить до достовірного зменшення виразності больового синдрому, скутості та функціональної недостатності суглобів за показниками болю за ВАШ, а також індексами WOMAC та Лекена.
- На фоні проведеної терапії у хворих з поєднаним перебігом ОА, ЦД 2-го типу та ожирінням було відмічене покращення показників рівня прозапальних цитокінів та рівня СРП.
- У хворих на ОА незалежно від ступеня ожиріння було визначено позитивну динаміку перебігу захворювання, однак більш виразною вона була у пацієнтів з І-м та ІІ-м ступенем ожиріння.
- При оцінюванні дінаміки показників вуглеводного обміну на фоні проведеної терапії не виявила погіршення перебігу ЦД 2-го типу.
Треба зазначити, відмічений позитивний вплив прийому діацереїну на перебіг ОА у хворих на ЦД 2-го типу із супутнім ожирінням. Крім того препарат має задовільну переносимість. Однак для підтвердження отриманих даних необхідно проведення подальших більш тривалих досліджень.
Стаття надана мовою оригіналу





